题目内容
NA表示阿伏加德罗常数,下列叙述正确的是
| A.1molC2H6中共价键数为8NA |
| B.3.2 g O2和O 3的混合气中氧原子数为0.2NA |
| C.1L 0.1mol·L-1Al2(SO4)3溶液中Al3+数为0.2NA |
| D.标准状况下,22.4 L甲醇的分子数为NA |
B
解析试题分析:A、1molC2H6中共价键数为7NA,A不正确;B、氧气和臭氧互为同素异形体,则3.2 g O2和O 3的混合气中氧原子的物质的量是3.2g÷16g/mol=0.2mol,其原子数为0.2NA,B正确;C、硫酸铝溶液中铝离子水解,因此1L 0.1mol·L-1Al2(SO4)3溶液中Al3+数小于0.2NA,C不正确;D、标准状况下,甲醇不是气态,不能适用于气体摩尔体积,D不正确,答案选B。
考点:考查阿伏伽德罗常数的有关计算

练习册系列答案
相关题目
下列有关化学用语表示正确的是
A.水的电子式: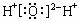 |
B.中子数为20的氯原子: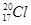 |
C.聚丙烯的结构简式: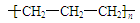 |
D.钠原子的结构示意图: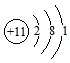 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,11.2L正丁烷所含共用电子对数为7NA |
| B.常温常压下,5.6g乙烯与丁烯的混合物中含有氢原子的数目为0.8NA |
| C.在50g质量分数为56%的乙醇水溶液中,含有氢原子总数为3NA |
D.将CO2通过Na2O2使其增重a g时,反应中转移电子数为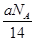 |
设NA为阿伏加德罗常数的数值,下列叙述正确的是(相对原子量:H—1 C—12)( )
| A.1 mol/L氯化铜溶液中的Cu2+数小于NA |
| B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA |
| C.28 g聚乙烯含有的碳原子数为2NA |
| D.1 mol CH5+所含电子数为8NA |
下列说法正确的是( )
| A.4.2 g丙烯中所含的共价键数目为0.6×6.02×1023 |
| B.含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为6.02×1023 |
| C.相同条件下,1 L CO和H2的混合气体完全燃烧消耗0.5 L O2 |
| D.相同物质的量的OH-和CH3+含有相同数目的电子 |
下列叙述正确的是( )
| A.含1 mol溶质的任何溶液,物质的量浓度一定相等 |
| B.配制1 mol·L-1NaCl溶液1 L,其方法是:将58.5 g NaCl溶于1 L水中 |
| C.体积相同、物质的量浓度相同的同种溶液所含溶质的粒子数一定相同 |
| D.1 L 0.5 mol·L-1 CaCl2溶液中,Ca2+与Cl-的物质的量浓度都是0.5 mol·L-1 |
若用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A.1 mol BrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA |
| B.锌与一定浓度的浓硫酸反应,产生标准状况下SO2和H2的混合气体22.4 L,锌失去电子数为2NA |
| C.常温常压下,20 g D2O含有的原子总数为3NA |
| D.标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数小于2NA |
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为( )。
| A.3.2 g | B.4.0 g | C.4.2 g | D.4.6 g |
设NA为阿伏加德罗常数的值,下列说法正确的是( )。
| A.某温度下,1 L pH=8的纯水中含OH-为10-8NA |
| B.14 g分子通式为CnH2n的链烃中含有的C=C键数目为NA |
| C.标准状况下,22.4 L Cl2与足量Fe反应,转移的电子数为3NA |
| D.常温下,1 L 0.1 mol·L-1 CH3COONa溶液中含有的Na+和CH3COO-总数为0.2NA |