题目内容
已知某二元酸H2A在水溶液中的电离方程式:
H2A=H++HA-,HA-![]() H++A-
H++A-
测得25℃时0.1mol·L-1的H2A溶液中,c(H+)=0.11mol·L-1,则该条件下,HA-的电离度是
[ ]
|
A.1% |
B.9.1% |
|
C.10% |
D.55% |
答案:C
解析:
提示:
解析:
|
【巧解导析】由H2A的电离方程式: H2A 设HA-的电离度为α,则由电离度的概念知: H2A 0.1mol 0.1mol 0.1mol HA- 0.1αmol 0.1αmol 0.1+0.1α=0.11(溶液中H+浓度) 即α=0.1=10%. |
提示:
|
【巧解点悟】电离度的概念课本上并没有给出,但它往往以信息的形式给出.本题的解题关键点是:必须分析题目所给两个电离方程式,弄清它们电离程度不同:“ |

练习册系列答案
相关题目
 H++HA-,HA-
H++HA-,HA-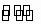 H++A2-知H2A的第一级电离是完全电离,而第二级电离是不完全电离,存在电离平衡,溶液中的H+是由这两步电离产生的.
H++A2-知H2A的第一级电离是完全电离,而第二级电离是不完全电离,存在电离平衡,溶液中的H+是由这两步电离产生的. ×100%=55%,即易误造D.
×100%=55%,即易误造D.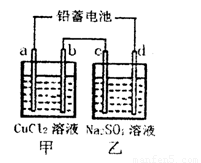
 2PbSO4(s)+2H2O(1)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是____________
2PbSO4(s)+2H2O(1)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是____________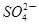 (aq)+4e-
(aq)+4e- PbSO4(s)+2H2O(1)
PbSO4(s)+2H2O(1) H++A2-,请回答下列问题:
H++A2-,请回答下列问题: H++A2-
H++A2- 2PbSO4(s) +2H2O(l)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是____________(填写序号)。
2PbSO4(s) +2H2O(l)。电解一段时间后,向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是____________(填写序号)。 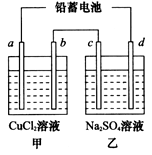
 H++A2-。
H++A2-。  CH3OH(g) △H=-90.8kJ/mol
CH3OH(g) △H=-90.8kJ/mol  CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol  CO2(g)+H2(g) △H=-41.3kJ/mol
CO2(g)+H2(g) △H=-41.3kJ/mol  2SO3(g)。在一定温度下,将0.23molSO2和0.11molO2通入容积为1L的密闭容器中发生反应,达到平衡后得到0.12molSO3,则反应的平衡常数K=__________。若温度不变,再通入0.50molO2后重新达到平衡,则SO3的体积分数将__________(填“增大”“不变”或“减小”)。
2SO3(g)。在一定温度下,将0.23molSO2和0.11molO2通入容积为1L的密闭容器中发生反应,达到平衡后得到0.12molSO3,则反应的平衡常数K=__________。若温度不变,再通入0.50molO2后重新达到平衡,则SO3的体积分数将__________(填“增大”“不变”或“减小”)。