题目内容
某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
|
方案 |
反应物 |
|
甲 |
Cu、浓HNO3 |
|
乙 |
Cu、稀HNO3 |
|
丙 |
Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象 ;但此实验的不足之处是 。
(1)检查装置气密性。(2)Cu+4HNO3(浓) Cu(NO3)2+2NO2↑+2H2O 反应变缓,气体颜色变淡。(3)丙;耗酸量最少,无污染。(4)向d中加入KBr溶液,c中加入固体KMnO4,由a向c中加入浓盐酸;c中有黄绿色气体产生,d中溶液变为黄棕色;没有处理尾气。
Cu(NO3)2+2NO2↑+2H2O 反应变缓,气体颜色变淡。(3)丙;耗酸量最少,无污染。(4)向d中加入KBr溶液,c中加入固体KMnO4,由a向c中加入浓盐酸;c中有黄绿色气体产生,d中溶液变为黄棕色;没有处理尾气。
【解析】
试题分析:(1)根据实验操作可知,目的是检查装置气密性。
(2)硝酸具有强氧化性,和铜反应的化学方程式是Cu+4HNO3(浓) Cu(NO3)2+2NO2↑+2H2O;加入蒸馏水后硝酸的浓度降低,反应变缓。同时由于稀硝酸的还原产物是NO,所以气体的颜色变浅。
Cu(NO3)2+2NO2↑+2H2O;加入蒸馏水后硝酸的浓度降低,反应变缓。同时由于稀硝酸的还原产物是NO,所以气体的颜色变浅。
(3)铜不论是和稀硝酸,还是和浓硝酸反应硝酸都没有完全转化为硝酸铜,且都生成污染性气体NO或NO2。而铜先生成氧化铜后,再和硝酸反应,一方面硝酸的利用率高,其次不会生成污染性气体,所以最佳方案是丙。
(4)要用上述装置进行实验证明氧化性KMnO4>Cl2>Br2,则应该利用酸性高锰酸钾溶液氧化浓盐酸生成氯气,然后再将生成的氯气通入到溴化钾溶液中即可。所以正确的操作是向d中加入KBr溶液,c中加入固体KMnO4,由a向c中加入浓盐酸;则相应的实验现象是c中有黄绿色气体产生,d中溶液变为黄棕色;由于氯气或单质溴都是有毒物质,因此该装置的不足是没有进行尾气处理。
考点:考查装置气密性的检验、硝酸铜的制备、氧化性强弱比较以及尾气处理等。
点评:该题是高考中的常见题型,试题综合性强,注重基础和能力的双向考查。该题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。

(12分)某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
| 方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象 ;但此实验的不足之处是 。
(12分)某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象 ;但此实验的不足之处是 。
(12分)某兴趣小组设计出下图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
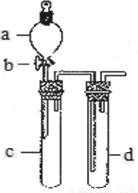
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是 。再由a向c中加2 mL蒸馏水,c中的实验现象是 。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 。理由是_____________。
|
方案 |
反应物 |
|
甲 |
Cu、浓HNO3 |
|
乙 |
Cu、稀HNO3 |
|
丙 |
Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为 ,实验现象 ;但此实验的不足之处是 。


