题目内容
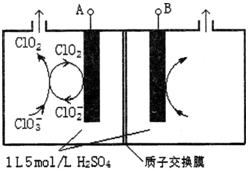
炼金废水中含有络离子[Au(CN)2]+,其电离出的CN—有毒,CN-与H+结合生成HCN时,其毒性更强。回答下列问题:
(1)HCN的电离方程式为______________________NaCN溶液的pH_____7(填“< > =”)
(2)与弱电解质的电离方程式相似,[Au(CN)2]+也存在着两步电离,其一级电离方程式为_________
(3)处理这种废水是在碱性条件下,NaClO将CN—氧化为碳酸根和氮气,其离子方程式为:__________
(4)在酸性条件下,ClO—也能氧化CN--,但实际处理废水时却不在酸性条件下进行的原因是_______________
(1)HCN的电离方程式为______________________NaCN溶液的pH_____7(填“< > =”)
(2)与弱电解质的电离方程式相似,[Au(CN)2]+也存在着两步电离,其一级电离方程式为_________
(3)处理这种废水是在碱性条件下,NaClO将CN—氧化为碳酸根和氮气,其离子方程式为:__________
(4)在酸性条件下,ClO—也能氧化CN--,但实际处理废水时却不在酸性条件下进行的原因是_______________
(1)HCN H++CN-,>;(2)[Au(CN)2]+
H++CN-,>;(2)[Au(CN)2]+ [Au(CN)] 2++CN-;
[Au(CN)] 2++CN-;
(3)5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O;
(4)在酸性条件下CN-与H+结合生成毒性很强的HCN,对人体造成危害。
 H++CN-,>;(2)[Au(CN)2]+
H++CN-,>;(2)[Au(CN)2]+ [Au(CN)] 2++CN-;
[Au(CN)] 2++CN-;(3)5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O;
(4)在酸性条件下CN-与H+结合生成毒性很强的HCN,对人体造成危害。
试题分析:(1)HCN是弱酸,在溶液中存在电离平衡,其电离方程式为HCN
 H++CN-;(2) [Au(CN)2]+存在着两步电离,其一级电离方程式为[Au(CN)2]+
H++CN-;(2) [Au(CN)2]+存在着两步电离,其一级电离方程式为[Au(CN)2]+ [Au(CN)] 2++CN-;(3)处理含有络离子[Au(CN)2]+废水是在碱性条件下,NaClO将CN—氧化为碳酸根和氮气,根据离子方程式的书写原则,该反应的离子方程式为:5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O;(4)在酸性条件下,ClO—也能氧化CN--,但实际处理废水时却不在酸性条件下进行是因为在酸性条件下CN-与H+结合生成毒性很强的HCN,对人体造成更大的危害。
[Au(CN)] 2++CN-;(3)处理含有络离子[Au(CN)2]+废水是在碱性条件下,NaClO将CN—氧化为碳酸根和氮气,根据离子方程式的书写原则,该反应的离子方程式为:5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O;(4)在酸性条件下,ClO—也能氧化CN--,但实际处理废水时却不在酸性条件下进行是因为在酸性条件下CN-与H+结合生成毒性很强的HCN,对人体造成更大的危害。
练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
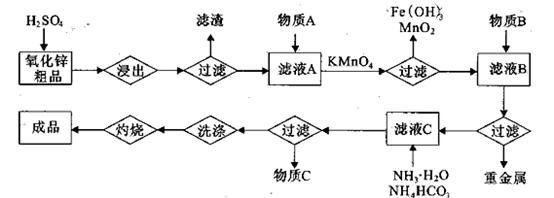
 +、Mn2+等
+、Mn2+等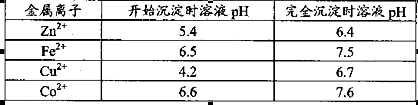
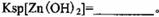 。
。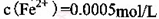 ,则处理1
,则处理1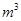 该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。
该溶液,Fe2+所消耗的KMnO4的质量为________g(保留两位有效数字)。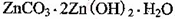 ,生成该沉淀的化学方程式为________。
,生成该沉淀的化学方程式为________。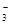 、K+
、K+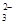 +H2O
+H2O