题目内容
0.01mol某烃与标准状况下2.02L氧气点燃恰好反应生成CO2、CO和水蒸气,将产物通过浓硫酸,浓硫酸增重0.9g;再通过灼热的氧化铜粉末,充分反应后,氧化铜质量减少0.48g。求该烃的分子式。
C8H10
解析:
(1)设产生CO的物质的量为x。
CuO+CO![]() Cu+CO2 Δm
Cu+CO2 Δm
80g 1mol 64g 16g
X 0.48 g
得x=0.03 mol。
(2)设该烃的分子式为CxHy。
已知:烃为0.01mol;n(O2)=![]() =0.09mol,
=0.09mol,
n(CO)=0.03mol,n(H2O)=![]() =0.05mol。
=0.05mol。
由O原子守恒求n(CO2):
0.09mol×2=2n(CO2)+0.03mol+0.05mol,
得n(CO2)=0.05mol。
0.01CxHy+0.09O2→0.05CO2+0.03CO+0.05H2O
根据C、H原子守恒得
得x=8,y=10。
即此烃分子式为C8H10。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
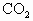 、CO和水蒸气,将产物都通过浓硫酸,浓硫酸增重0.9g,剩余气体通过灼烧的氧化铜粉末,充分反应之后,氧化铜质量减少了0.48g,求烃的分子式.
、CO和水蒸气,将产物都通过浓硫酸,浓硫酸增重0.9g,剩余气体通过灼烧的氧化铜粉末,充分反应之后,氧化铜质量减少了0.48g,求烃的分子式.