题目内容
下列叙述不正确的是 ( )
| A.Na、Mg、Al的第一电离能依次减弱 |
| B.H2S、H2O、HF的稳定性依次增强 |
| C.NaOH、Mg(OH)2、Al(OH)3的碱性依次减弱 |
| D.H4SiO4、H2CO3、H2SO4酸性依次增强 |
A
解析试题分析:镁的3s轨道电子处于全充满状态,稳定性其余,所以镁的第一电离能大于Al的,A不正确;非金属性越强,氢化物的稳定性越强,B正确;金属性或非金属性越强,最高价氧化物的水化物碱性或酸性越强,所以选项CD正确,答案选A。
考点:考查元素周期律的应用和判断
点评:该题是高考中的常见题型和考点,属于中等难度试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,主要是考查学生灵活运用元素周期律知识解决实际问题的能力,有利于培养学生的逻辑推理能力和应试能力,提高学生的学科素养。

练习册系列答案
相关题目
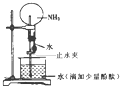 如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )
如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )| A、该实验说明氨气是一种极易溶于水的气体 | B、进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性 | C、氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化 | D、形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压 |
苯与乙烯相比较,下列叙述不正确的是( )
| A、都能燃烧,生成二氧化碳和水 | B、都容易发生加成反应 | C、乙烯易发生加成反应,苯只能在特殊条件下才发生加成反应 | D、乙烯易被酸性高锰酸钾溶液氧化,苯不能被酸性高锰酸钾溶液氧化 |