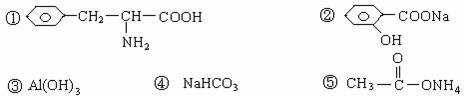题目内容
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)________。
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
A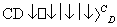 B(在水溶液中进行)
B(在水溶液中进行)
其中C是溶于水显酸性的气体;D是淡黄色固体。
写出C的结构式________;D的电子式_______ _。
_。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为____________;由A转化为B的离子方程式为_____________________________________________。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:________________________________________。A、B浓度均为0.1 mol·L-1的混合溶液中,离子浓度由大到小的顺序是__________________;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有_______________________________。
解析:本题考查物质结构、元素周期律及化学方程式的书写等,意在考查考生的分析推理能力。首先根据题意可推出五种元素依次是H、C、O、Na、Al。(1)根据“同周期元素从左向右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大”即可解答。(2)五种元素形成的气体溶于水呈酸性,则C只能是CO2,淡黄色固体D只能是Na2O2。①根据信息可知B是Al(OH)3,在水溶液中Na2O2与水反应生成NaOH,再与Al(OH)3反应生成NaAlO2,故A是NaAlO2。将CO2通入NaAlO2溶液中,若CO2过量生成NaHCO3,若CO2不足则生成Na2CO3。②易推出A是Na2CO3,B是NaHCO3。等物质的量浓度的Na2CO3与NaHCO3的混合溶液中,c(Na+)最大;由于CO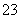 的水解程度大于HCO
的水解程度大于HCO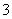 且前者水解生成后者,所以c(HCO
且前者水解生成后者,所以c(HCO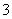 )>c(CO
)>c(CO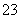 );溶液呈碱性则必有c(OH-)>c(H+);又由于OH-和H+均来自弱电解质的电离或水解,其浓度很小,则有c(Na+)>c(HCO
);溶液呈碱性则必有c(OH-)>c(H+);又由于OH-和H+均来自弱电解质的电离或水解,其浓度很小,则有c(Na+)>c(HCO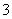 )>c(CO
)>c(CO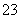 )>c(OH-)>c(H+)。向该溶液中滴加盐酸,发生反应:Na2CO3+HCl===NaHCO3+NaCl,NaHCO3+HCl===NaCl+H2O
)>c(OH-)>c(H+)。向该溶液中滴加盐酸,发生反应:Na2CO3+HCl===NaHCO3+NaCl,NaHCO3+HCl===NaCl+H2O +CO2↑,少量二氧化碳溶于水使溶液呈酸性,所以当溶液呈中性时,应有少量NaHCO3剩余,因此溶质的主要成分是NaHCO3、NaCl和CO2(或H2CO3)。
+CO2↑,少量二氧化碳溶于水使溶液呈酸性,所以当溶液呈中性时,应有少量NaHCO3剩余,因此溶质的主要成分是NaHCO3、NaCl和CO2(或H2CO3)。
答案:(1)Na>Al>C>O>H
(2)O===C===O Na+[∶O∶,∶∶O∶,∶∶]2-Na+
①NaAlO2 AlO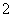 +2H2O+CO2===Al(OH)3↓+HCO
+2H2O+CO2===Al(OH)3↓+HCO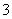 (或2AlO
(或2AlO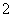 +3H2O+CO2===2Al(OH)3↓+CO
+3H2O+CO2===2Al(OH)3↓+CO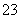 )
)
②CO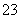 +H2OHCO
+H2OHCO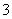 +OH- c(Na+)>c(HCO
+OH- c(Na+)>c(HCO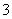 )>c(CO
)>c(CO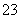 )>c(OH-)>c(H+) NaCl、NaHCO3、CO2(或H2CO3)
)>c(OH-)>c(H+) NaCl、NaHCO3、CO2(或H2CO3)

 名校课堂系列答案
名校课堂系列答案已知几种短周期元素的原子半径、常见的最高价和最低价如下表,下列说法中不正确的是 ( )
| 元素性质 | 元素编号 | ||||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 原子半径(nm) | 0.073 | 0.075 | 0.152 | 0.110 | 0.099 | 0.186 | 0.143 |
| 最高正化合价 | 无 | +5 | +1 | +5 | +7 | +1 | +3 |
| 最低负化合价 | -2 | -3 | 无 | -3 | -1 | 无 | 无 |
A.⑦的简单离子不是同周期元素离子半径最小的
B.气态氢化物的稳定性①>②
C.②的气态氢化物浓溶液可用于检验氯气管道的泄漏
D.阴离子的还原性④大于⑤,最高价氧化物的水化物的碱性③小于⑥
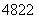 Ti和
Ti和 Ti的说法中正确的是( )
Ti的说法中正确的是( )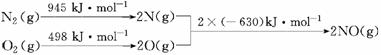
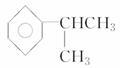 名称是________。
名称是________。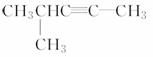 分子式为________。名称是________,1 mol该烃完全燃烧耗O2________mol。
分子式为________。名称是________,1 mol该烃完全燃烧耗O2________mol。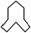 名称是________。
名称是________。