题目内容
已知X、Y、Z都是有刺激性气味的气体,M是一种金属单质,D是一种盐.有以下转化关系,部分产物未标出.
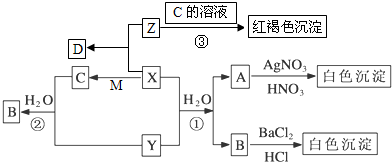
试回答:
(1)写出下列物质的化学式
X 、Y 、Z 、M 、D .
(2)写出下列反应的离子方程式
① ,
② ,
③ .

试回答:
(1)写出下列物质的化学式
X
(2)写出下列反应的离子方程式
①
②
③
考点:无机物的推断
专题:推断题
分析:X、Z都是有刺激性气味的气体,D是一种盐,D为铵盐,Z和C反应生成红褐色沉淀,则Z为NH3,B为可溶性铁盐,M是金属单质,能和X生成可溶性铁盐,根据元素守恒知,M是Fe,能将铁氧化为最高价的有刺激性气味的气体是氯气,所以X是Cl2,氯气和Y、水反应生成A和B,A能和硝酸酸化的硝酸银溶液反应生成白色沉淀,则A中含有氯离子,B能和盐酸酸化的氯化钡反应生成白色沉淀,则B中含有硫酸根离子,根据元素守恒及物质的性质知,Y为SO2,氯气和氨气反应生成铵盐D,根据元素守恒知,D为NH4Cl,二氧化硫、氯化铁发生氧化还原反应生成亚铁离子和硫酸,所以B为硫酸.
解答:
解:X、Z都是有刺激性气味的气体,D是一种盐,D为铵盐,Z和C反应生成红褐色沉淀,则Z为NH3,B为可溶性铁盐,M是金属单质,能和X生成可溶性铁盐,根据元素守恒知,M是Fe,能将铁氧化为最高价的有刺激性气味的气体是氯气,所以X是Cl2,氯气和Y、水反应生成A和B,A能和硝酸酸化的硝酸银溶液反应生成白色沉淀,则A中含有氯离子,B能和盐酸酸化的氯化钡反应生成白色沉淀,则B中含有硫酸根离子,根据元素守恒及物质的性质知,Y为SO2,氯气和氨气反应生成铵盐D,根据元素守恒知,D为NH4Cl,二氧化硫、氯化铁发生氧化还原反应生成亚铁离子和硫酸,所以B为硫酸
(1)通过以上分析知,X、Y、Z、M、D分别是Cl2、SO2、NH3、Fe、NH4Cl,
故答案为:Cl2;SO2;NH3;Fe;NH4Cl;
(2)X是氯气、Y是二氧化硫,二者在水溶液里发生氧化还原反应生成盐酸和硫酸,离子方程式为Cl2+SO2+2H2O=2Cl-+SO4 2-+4H+,
C是氯化铁、Y是二氧化硫,氯化铁溶液和二氧化硫发生氧化还原反应生成亚铁离子和硫酸,离子方程式为:2Fe 3++SO2+2H2O=2Fe 2++SO42-+4H+,
Z是氨气、C是氯化铁,二者反应生成氢氧化铁和氯化铵,离子方程式为:Fe 3++3NH3+3H2O=Fe(OH)3↓+3NH4+,
故答案为:Cl2+SO2+2H2O=2Cl-+SO4 2-+4H+;
2Fe 3++SO2+2H2O=2Fe 2++SO42-+4H+;
Fe 3++3NH3+3H2O=Fe(OH)3↓+3NH4+.
(1)通过以上分析知,X、Y、Z、M、D分别是Cl2、SO2、NH3、Fe、NH4Cl,
故答案为:Cl2;SO2;NH3;Fe;NH4Cl;
(2)X是氯气、Y是二氧化硫,二者在水溶液里发生氧化还原反应生成盐酸和硫酸,离子方程式为Cl2+SO2+2H2O=2Cl-+SO4 2-+4H+,
C是氯化铁、Y是二氧化硫,氯化铁溶液和二氧化硫发生氧化还原反应生成亚铁离子和硫酸,离子方程式为:2Fe 3++SO2+2H2O=2Fe 2++SO42-+4H+,
Z是氨气、C是氯化铁,二者反应生成氢氧化铁和氯化铵,离子方程式为:Fe 3++3NH3+3H2O=Fe(OH)3↓+3NH4+,
故答案为:Cl2+SO2+2H2O=2Cl-+SO4 2-+4H+;
2Fe 3++SO2+2H2O=2Fe 2++SO42-+4H+;
Fe 3++3NH3+3H2O=Fe(OH)3↓+3NH4+.
点评:本题考查了无机物推断,根据物质的颜色、物质的特殊气味等为突破口,采用正逆结合的方法进行推断,再结合物质的氧化性、还原性解答,题目难度中等.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
| B、浓H2SO4有强氧化性,常温下不与Fe、Al发生反应 |
| C、金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
| D、将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
元素的以下性质,随着原子序数的递增不呈周期性变化的是( )
| A、化合价 |
| B、原子半径 |
| C、相对原子质量 |
| D、金属性和非金属性 |
由长周期元素和短周期元素共同构成的族是( )
①0族 ②主族 ③副族 ④第Ⅷ族.
①0族 ②主族 ③副族 ④第Ⅷ族.
| A、①② | B、①③ | C、②③ | D、③④ |
常温下,下列溶液中各组离子一定能大量共存的是( )
| A、使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32- | ||
| B、由水电离产生的c(H+)=10-12mol?L-1的溶液:NH4+、SO42-、HCO3-、Cl- | ||
| C、含有0.1 mol?L-1 HCO3-的溶液:Na+、Fe3+、NO3-、SCN- | ||
D、
|

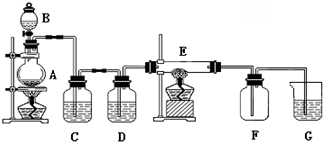
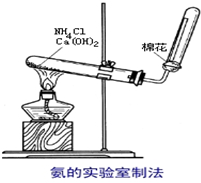 如图为实验室制取氨的实验装置.
如图为实验室制取氨的实验装置. 根据如图所示的装置,回答下列问题:
根据如图所示的装置,回答下列问题: