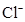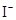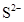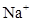题目内容
1 mol?L-1 NaCl溶液的含义是
| A.1 L水中含有1 mol NaCl | B.溶液中含有1 mol NaCl |
| C.1 L溶液中含有58.5 g NaCl | D.将58.5 g NaCl溶于1 L水中所得的溶液 |
C
解析试题分析:溶质的物质的量浓度的概念为:单位体积溶液中含有溶质的物质的量,1mol/L NaCl溶液的含义是:1L氯化钠溶液中含有溶质NaCl的物质的量为1mol。A、1 mol?L-1 NaCl溶液是1 L溶液中含有1mol NaCl,不是1L水中含有1mol NaCl,错误;B、没有指出溶液的体积,错误;C、1mol/L NaCl溶液的含义是:1L氯化钠溶液中含有溶质NaCl的物质的量为1mol,质量为58.5 g,正确;D、将58.5 g NaCl溶于1 L水中所得的溶液的体积不是1L,溶液的浓度不是1mol/L,错误。
考点:考查物质的量浓度的概念。

练习册系列答案
相关题目
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.室温下H2O2分解得到16 g O2,转移的电子数为2NA |
| B.含1mol H2SO4的浓硫酸与足量铜反应转移的电子总数为NA |
| C.标准状况下11.2 L CO和H2的混合气体完全燃烧消耗O2的量为0.25NA |
| D.相同物质的量OH-和CH3+含有相同数目的电子 |
有甲、乙、丙三瓶等体积等物质的量浓度的NaOH溶液,若将甲蒸发掉一半水分,在乙中通入少量的CO2,丙不变,然后分别向甲、乙、丙三瓶中加入同浓度的盐酸,完全反应后所需盐酸溶液的体积是 ( )
| A.甲=丙>乙 | B.丙>乙>甲 | C.乙>甲=丙 | D.甲=乙=丙 |
下列化学用语正确的是
| A.乙烯的结构简式:CH2CH2 |
B.氟原子的结构示意图: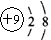 |
C.甲烷的电子式: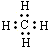 |
| D.碳酸钠的电离方程式:Na2CO3=Na++CO32- |
设NA代表阿伏加德罗常数的数值,下列说法中正确的是( )
| A.1.8 g重水(D2O)中含有的质子数和电子数均为1.0NA |
| B.0℃、1个标准大气压下,22.4L NO 和22.4L O2混合后所得气体中分子总数为1.5NA |
| C.含4mol Si-O键的二氧化硅晶体中,氧原子数为2NA |
| D.将11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA |
下列有关化学用语表示正确的是
A.钾原子结构示意图: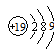 |
B.间羟基苯甲酸的结构简式: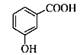 |
C.CO2的比例模型: |
D.Na2S的电子式: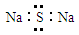 |
用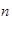 A表示阿伏加德罗常数的值。下列说法正确的是
A表示阿伏加德罗常数的值。下列说法正确的是
A.1 mol Cl-离子中含有的电子数为8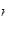 A A |
B.标准状况下,2.24 L H20中含有的分子数为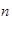 A A |
C.27g铝与足量的氧气反应,转移的电子数为3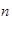 A A |
D.0.2 mo1·L-1 Ca(NO3)2溶液中含有的N03-离子数为0.4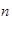 A A |
下列有关化学用语的表述正确的是( )
| A.原子核内有8个中子的碳原子148C |
B.钠离子的结构示意图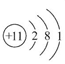 |
C.H2O的电子式: |
| D.乙醇的分子式:C2H6O |
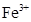 、
、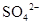 、
、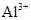 和M离子,且
和M离子,且