题目内容
【题目】欲配制1.00mol/L的NaCl溶液1000mL,需要使用的仪器和药品是( )
A.500mL容量瓶,58.5gNaClB.1000mL容量瓶,58.5gNaCl
C.500mL容量瓶,117gNaClD.1000mL容量瓶,117 gNaCl
【答案】B
【解析】
配制1.00mol/L的NaCl溶液1000mL,选用1000mL容量瓶,需要NaCl的质量m=nM= cVM =1.00mol/L×1.0L×58.5g/mol=58.5g,答案选B。

【题目】大量排放氮的氧化物会产生酸雨、光化学烟雾等环境问题。工业上处理氮的氧化物途径有多种:
Ⅰ.碱吸祛。利用纯碱溶液吸收NO、NO2,发生的反应有:
2NO2+Na2CO3=NaNO3+NaNO2+CO2,NO+NO2+Na2CO3=2NaNO2+CO2
用一定量纯碱溶被吸收NO、NO2恰好完全反应得到吸收溶液。
(1)向吸收溶液中滴加酸性高锰酸钾溶液,溶液褪色,氧化产物为NO3-,写出离子方程式__________
Ⅱ.天然气还原法。
CH4催化还原NO、NO2的热化学方程式如下:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574k]/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH2=-1160kJ/mol
(2)4NO(g)=N2(g)+2NO2(g)ΔH=_________
(3)上述物质NaNO2、NO、CO2中含有共同的化学键的类型是_______
Ⅲ.活性炭还原法。
在VL恒容密闭容器中加入足量的活性炭和一定量NO,恒温(T1)条件下发生反应生成Q、P(均为无污染物质)。测得物质的量与时间关系如表所示:
n/mol t/min | NO | Q | P |
0 | 0.200 | 0 | 0 |
10 | 0.116 | 0.042 | 0.042 |
20 | 0.080 | 0.060 | 0.060 |
30 | 0.080 | 0.060 | 0.060 |
(4)在T1温度下,NO的平衡转化率为_______;平衡常数K为_________(用分数表示)。
(5)30min后,将温度升高至T2达到平衡时,容器中NO、Q、P的浓度之比为3:1:1,则该反应的正反应ΔH_____0(填“>”“<”或“=”)。在T2温度达到平衡之后,再向容器中充入少量NO,则NO的平衡转化率将_____________“变大”“不变”“变小”)。
【题目】乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。裂解的副反应为C4H10(g,正丁烷) ![]() CH4(g)+C3H6(g)
CH4(g)+C3H6(g)
请回答下列问题
(1)化学上,将稳定单质的能量定为0,由元素的单质化合成单一化合物时的反应热叫该化合物的生成热,生成热可表示该物质相对能量。25℃、101kPa几种有机物的生成热如下表所示:
物质 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
生成热/ kJ·mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
由正丁烷裂解生成乙烯的热化学方程式为_______________________________。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。
①下列情况能说明该反应达到平衡状态的是__________(填标号)
A.气体密度保持不变 B.c(C2H4)·c(C2H6)/c(C4H10)保持不变
C.反应热保持不变 D.正丁烷分解速率利乙烷消耗速率相等
②为了提高反应速率和反应物的转化率,可采收的措施是______________________________。
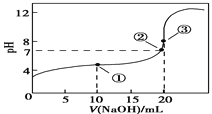
(3)向密闭容器中充入正丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,随着温度升高,乙烯产率降低,可能的原因是____________________________________________。

(4)在一定温度下向10L恒容密闭容器中充入2mol正丁烷,反应生成乙烯和乙烷,经过10min达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10min内乙烷的生成速率v(C2H6)=__________ mol·L-1·min-1
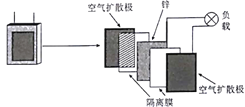
②上述条件下,正丁烷的平衡转化率为______________,该反应的平衡常数K为____________。 (5)丁烷一空气燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的正极反应式为26CO2+13O2+52e-=26CO32-,则负极反应式为_______________________。