题目内容
工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:

已知: Cu2O + 2H+ = Cu + Cu2+ + H2O
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 。
(2)反应Ⅰ完成后,铁元素的存在形式为 。(填离子符号)
请写出生成该离子的离子方程式 。
(3)x、y对应的数值范围分别是 、 。
(4)下列关于NaClO调pH的说法正确的是 。
a. 加入NaClO可使溶液的pH降低
b. NaClO能调节pH的主要原因是由于发生反应ClO-+ H+ HClO,
HClO,
ClO-消耗H+,从而达到调节pH的目的
c .NaClO能调节pH的主要原因是由于NaClO水解ClO-+ H2O HClO+OH-,
HClO+OH-,
OH-消耗H+ ,从而达到调节pH的目的
(5)用NaClO调pH,写出氯气制取漂白液的离子方程式: 。
(1)SiO2、Cu(各1分)
(2)Fe2+ (2分)
2Fe3+ + Cu = Cu2+ + 2Fe2+(2分)
(3)3.2≤pH<4.0 5.2≤pH<5.4(各1分)
(4)b (2分)
(5)5ClO-+ 2Fe2+ + 5H2O = 2Fe(OH)3 + Cl-+ 4HClO(2分)
(或 2Fe2+ +7ClO-+ 2H++ 5H2O = 2Fe(OH)3 + Cl-+ 6HClO)

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
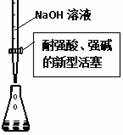
课课通课程标准思维方法与能力训练系列答案下图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是
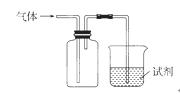
| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A. | NO | 紫色石蕊试液 | 溶液变红 | NO与水反应生成硝酸 |
| B. | C2H4 | 溴水 | 溶液褪色 | 乙烯能与溴发生加成反应 |
| C. | SO2 | 酸性KMnO4溶液 | 溶液褪色 | SO2有还原性 |
| D. | NH3 | MgCl2溶液 | 产生白色沉淀 | NH3有碱性 |
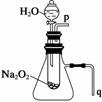
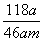 % B.
% B.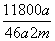 %
%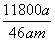 % D.
% D.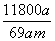 %
%
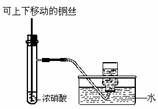

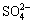 ,H2SO3,
,H2SO3,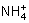 )分别进行如下实验:
)分别进行如下实验: