题目内容
用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是( )
①加盐酸溶解
②加烧碱溶液溶解
③过滤
④通入过量CO2生成Al(OH)3沉淀
⑤加入盐酸生成Al(OH)3沉淀
⑥加入过量烧碱溶液
| A.①⑥⑤③ | B.②③④③ | C.②③⑤③ | D.①③⑤③ |
B
解析

练习册系列答案
相关题目
现有下列物质:①纯碱 ②小苏打 ③Al(OH)3④Al2O3⑤FeO,其中既能与盐酸反应又能与NaOH溶液反应的是( )
| A.①②③ | B.②③④ | C.①③④ | D.①③⑤ |
有3份等质量的小苏打,第1份直接与盐酸恰好完全反应;第2份首先加热,使其部分分解后,再与盐酸恰好完全反应;第3份首先加热,使其完全分解后,再与盐酸恰好完全反应。假若盐酸的物质的量浓度相同,消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是( )。
| A.V1>V2>V3 | B.V1>V3>V2 |
| C.V2>V3>V1 | D.V1=V2=V3 |
红珊瑚栖息于200~2000 m的海域,产于台湾海峡、南中国海,它与琥珀、珍珠被统称为有机宝石。在中国,珊瑚是吉祥的象征,一直用来制作珍贵的工艺品。红珊瑚是无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,其红色是因为在海底长期积淀某种元素,该元素是( )
| A.Na | B.Fe | C.Si | D.Cu |
把一块镁铝合金投入到20 mL 1 mol/L的HCl溶液里,待合金完全溶解后,往溶液里加入1 mol/L的NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积(mL)变化的关系如图所示。下列说法中正确的是( )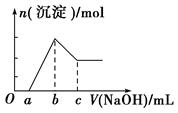
| A.镁铝合金具有很强的抗腐蚀能力,它不溶解在任何酸、碱或盐中 |
| B.c值越大,合金中Al的含量越高 |
| C.b值越大,合金中Mg的含量越高 |
| D.假设c=25,整个反应过程中,主要发生了5个离子反应 |
潜艇上的核反应堆使用液态铝钠合金(单质钠和单质铝熔合成)
作载热介质,下列有关说法正确的是( )
| A.该合金的熔点介于钠、铝之间 |
| B.钠或铝形成的氧化物均为碱性氧化物 |
| C.钠和铝分别与少量的盐酸反应,所得溶液均呈中性 |
| D.若合金中n(Na)>n(Al),将其投入到足量的水中可得无色透明溶液 |
将过量的CO2通入下列溶液中,最终不出现白色沉淀的是( )
| A.CaCl2溶液 | B.NaAlO2溶液 |
| C.饱和Na2CO3溶液 | D.水玻璃 |
1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是 ( )。
| A.Na2CO3 | B.Na2O2、Na2CO3 |
| C.NaOH、Na2CO3 | D.Na2O2、NaOH、Na2CO3 |
