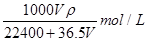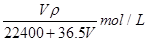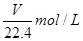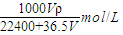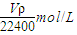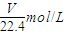题目内容
将标准状况下的V L HCl(气)溶于1000g水中,得到的盐酸密度为ρg/cm3,则该盐酸的物质的量浓度为( )
分析:根据n=
计算氯化氢的物质的量,再根据m=nM计算氯化氢质量,溶液的质量=1000g+m(HCl),结合密度求出溶液的体积,根据物质的量浓度公式c=
计算溶液的物质的量浓度.
| V |
| Vm |
| n |
| V |
解答:解:将标准状况下的V L HCl(气)的物质的量为
=
mol.
氯化氢的质量为
mol×36.5g/mol=
g.
所以溶液质量为1000g+
g=(1000+
)g.
所以溶液的体积为
=
ml=
×10-3L.
所以溶液浓度为
=
mol/L.
故选:A.
| VL |
| 22.4L/mol |
| V |
| 22.4 |
氯化氢的质量为
| V |
| 22.4 |
| 36.5V |
| 22.4 |
所以溶液质量为1000g+
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
所以溶液的体积为
(1000+
| ||
| ρg/ml |
| 22400+36.5V |
| 22.4ρ |
| 22400+36.5V |
| 22.4ρ |
所以溶液浓度为
| ||
|
| 1000Vρ |
| 22400+36.5V |
故选:A.
点评:本题考查物质的量浓度的相关计算与理解,难度不大,正确判断溶液的体积是解本题的关键,注意不能把溶剂的体积当做溶液的体积.也可计算质量分数,利用c=
计算.
| 1000ρω |
| M |

练习册系列答案
相关题目