题目内容
【题目】过氧化镁(MgO2)产品中常混有少量MgO,甲、乙两小组分别设计了两种实验方案测定样品中过氧化镁的质量分数。
方案Ⅰ:取一定量过氧化镁样品,加入少量的MnO2,搅拌使其充分混合,再向其中滴加足量的稀硫酸(如图)。

方案Ⅱ:称取0.1000g样品置于碘量瓶中,加入足量KI溶液和稀硫酸,滴加几滴指示剂X,摇匀后在暗处静置5 min,然后用0.1000 mol·L-1 Na2S2O3的标准溶液滴定至终点(如图),消耗Na2S2O3溶液30.00 mL。(已知:I2+2Na2S2O3=Na2S4O6+2NaI)

回答下列问题:
(1)方案Ⅰ实验前检验气密性的方法是________。仪器a的名称是________,使用该仪器的优点是________。
(2)广口瓶内发生的化学反应方程式为:MgO2+H2SO4=MgSO4+H2O2,________。
(3)方案Ⅱ滴定过程中若操作过慢,导致结果________(填“偏高”“偏低”或“无影响”)。指示剂X为________,判断到滴定终点的现象为________。
(4)根据方案Ⅱ实验数据,样品中过氧化镁的质量分数为________。
【答案】向量气管中加水到右端液面高出左端液面,一段时间后,若液面不发生变化,则气密性良好 恒压漏斗 使分液漏斗内的液体顺利滴下 2H2O2![]() 2H2O+O2↑ 偏高 淀粉溶液 溶液由蓝色变为无色(或“溶液褪色”),且半分钟内不变色 84%
2H2O+O2↑ 偏高 淀粉溶液 溶液由蓝色变为无色(或“溶液褪色”),且半分钟内不变色 84%
【解析】
本实验通过两组不同的实验测定样品中过氧化镁的质量分数。第一组实验通过过氧化镁、MnO2与稀硫酸的反应测定样品中过氧化镁的质量分数,通过测量生成气体的体积计算样品含量;第二组实验为滴定实验,过氧化镁具有氧化性,可以将KI中的I-还原出来,再通过测定溶液中I2的含量间接测定样品含量。
(1)实验装置连接好后,应检查装置气密性,方法是:向量气管中加水到右端液面高出左端液面,一段时间后,若液面不发生变化,则气密性良好;仪器A的名称是:恒压漏斗;使用恒压漏斗的优点是:使分液漏斗内的液体顺利滴下;
(2)广口瓶中发生两步化学反应,一是MgO2+H2SO4=MgSO4+H2O2,二是2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)过氧化镁具有氧化性,可以将碘化钾氧化生成碘单质,若滴定过程中操作过慢,碘化钾中的碘离子会被空气中的氧气氧化为碘单质,消耗硫代硫酸钠的标准溶液体积偏大,导致最终结果偏高;因溶液中有碘单质,则指示剂应选择淀粉溶液;滴定终点的现象为溶液由蓝色变为无色(或“溶液褪色”),且半分钟内不变色;
(4)过氧化镁氧化碘化钾的离子方程式为MgO2+2I-+4H+=Mg2++I2+2H2O,结合硫代硫酸钠与碘单质的反应可以得出过氧化镁与硫代硫酸钠的关系式为MgO2~2Na2S2O3,则n(MgO2)=![]() n(Na2S2O3)=
n(Na2S2O3)=![]() ×0.1000mol/L×0.03L=0.0015mol,m(MgO2)=0.0015mol×56g/mol=0.0840g,则样品中过氧化镁的质量分数=
×0.1000mol/L×0.03L=0.0015mol,m(MgO2)=0.0015mol×56g/mol=0.0840g,则样品中过氧化镁的质量分数=![]() =84%。
=84%。

 53天天练系列答案
53天天练系列答案【题目】在药物制剂中,抗氧剂与被保护的药物在与![]() 发生反应时具有竞争性,抗氧性强弱主要取决于其氧化反应的速率。
发生反应时具有竞争性,抗氧性强弱主要取决于其氧化反应的速率。![]() 、
、![]() 和
和![]() 是三种常用的抗氧剂。已知:
是三种常用的抗氧剂。已知:![]() 溶于水发生反应:
溶于水发生反应:![]() ;
;![]() 以原溶液和一定量的酸或碱混合,保持总体积不变的方式调节pH。
以原溶液和一定量的酸或碱混合,保持总体积不变的方式调节pH。
实验用品 | 实验操作和现象 |
| 实验1:溶液 |
| 实验2:溶液
|
| 实验3:调溶液 |
下列说法中不正确的是 ![]()
A.![]() 溶液显碱性,原因是
溶液显碱性,原因是![]()
B.![]() 溶液中
溶液中![]() 的电离程度大于水解程度
的电离程度大于水解程度
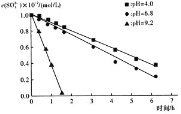
C.实验2说明,![]() 在
在![]() 时抗氧性最强
时抗氧性最强
D.实验3中,三种溶液在pH相同时起抗氧作用的微粒种类和浓度相同,因此反应速率相同