题目内容
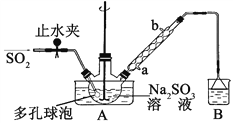
【题目】某探究小组为探究氯气的性质,设计了如下实验装置.请回答下列问题:
(1)装置A是用来制取氯气的,若烧瓶中盛放的是漂白粉,分液漏斗中是浓盐酸①配平该反应的化学方程式:
Ca(ClO)2+()═Cl2↑+CaCl2+()
②装置A中g管的作用是 .
(2)装置D中放有一块红色的纸条,一半用水润湿,一半干燥.实验过程中发现,湿润的部分很快褪色了,又过了一段时间,整块纸条全部褪色.某同学认为是因为装置D中下半部分氯气浓度大于上半部分,这种解释是否合理?(填“合理”或“不合理”),若不合理请说明真正的原因:(若填合理则此空不答).
(3)反应一段时间后用注射器从E中抽取少量溶液,检验出有Fe3+生成,请写出该反应的化学方程式:
(4)该装置缺少尾气处理装置,根据所学知识写出尾气处理的化学方程式: . 
【答案】
(1)1;4;HCl;2;1;2;H2O;平衡压强,使浓盐酸能顺利地滴入烧瓶中
(2)不合理;实验进行中氯气与湿润纸条中的水生成HClO,使纸条湿润部分褪色,干燥的部分无水,不能生成HClO所以不褪色,但过一段时间后由于水分子运动,整个纸条都变得湿润,所以就全部褪色了
(3)2FeCl2+Cl2═2FeCl3
(4)Cl2+2NaOH=NaCl+NaClO+H2O
【解析】解:(1)①反应中次氯酸钙中氯元素化合价变化为:+1→0,反应物中氯化氢化合价变化为:﹣1→0,依据氧化还原反应得失电子守恒,1molCa(ClO)2反应得到2mol电子,则被氧化的氯化氢的物质的量为2mol,生成氯气物质的量为2mol,依据原子个数守恒反应方程式:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O;所以答案是:1;4HCl;2;1;2H2O;②导气管将分液漏斗与圆底烧瓶相连,使二者内部压强相等,使浓盐酸能顺利地滴入烧瓶中;所以答案是:平衡压强,使浓盐酸能顺利地滴入烧瓶中;(2)实验进行中氯气与湿润纸条中的水生成HClO,使纸条湿润部分褪色,干燥的部分无水,不能生成HClO所以不褪色,但过一段时间后由于水分子运动,整个纸条都变得湿润,所以就全部褪色了;所以答案是:不合理; 实验进行中氯气与湿润纸条中的水生成HClO,使纸条湿润部分褪色,干燥的部分无水,不能生成HClO所以不褪色,但过一段时间后由于水分子运动,整个纸条都变得湿润,所以就全部褪色了;(3)氯气与氯化亚铁反应生成氯化铁,化学方程式:2Fe Cl2+Cl2═2FeCl3;所以答案是:2FeCl2+Cl2═2FeCl3;(4)氯气能够与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,可以用氢氧化钠溶液吸收氯气,化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O;所以答案是:Cl2+2NaOH=NaCl+NaClO+H2O.
【考点精析】解答此题的关键在于理解氯气的化学性质的相关知识,掌握氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应,以及对氯气的实验室制法的理解,了解实验室制法:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O.

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案