题目内容
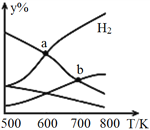
【题目】以二氧化碳和氢气为原料制取乙醇的反应为:2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )
CH3CH2OH(g)+3H2O(g) ΔH<0。某压强下的密闭容器中,按CO2和H2的物质的量比为1︰3投料,不同温度下平衡体系中各物质的物质的量百分数(y%)随温度变化如图所示。下列说法正确的是( )
A. a点的平衡常数小于b点
B. b点,υ正(CO2)=υ逆(H2O)
C. a点,H2和H2O物质的量相等
D. 其他条件恒定,充入更多H2,乙醇的物质的量分数增大
【答案】C
【解析】A、因为平衡常数仅与温度有关,该反应为放热反应,升高温度平衡向逆反应移动,所以温度越低,K越大,所以Ka>Kb,故A错误;B、b点时反应物仍然减小,生成物仍然增大,说明平衡向正反应方向进行,所以v正(CO2)≠v逆(H2O),故B错误;C、根据图象分析,a点为H2和H2O物质的量的交点,所以相等,故C正确;D、其他条件恒定,充入更多H2,气体的总物质的量的增大幅度更大,例如充入非常多的氢气,由于乙醇的物质的量的增量有限,乙醇的物质的量分数会减小,故D错误;故选C。

练习册系列答案
相关题目