题目内容
8.关于元素周期表的说法不正确的是( )| A. | 元素周期表有7个主族7个周期 | |
| B. | 原子最外电子层只有2个电子的元素可能是金属元素也可能是非金属元素 | |
| C. | 在元素周期表中位于金属元素和非金属元素交界处最容易找到耐高温耐腐蚀的合金材料 | |
| D. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 |
分析 A.根据周期表的结构分析;
B.第IIA族和He的最外层电子数均为2;
C.在元素周期表中位于金属元素和非金属元素交界处的元素具有半导体的性质;
D.从ⅢB族到ⅡB族10个纵行均为过渡元素.
解答 解:A.元素周期表有18个纵行,包括7个主族、7个副族、1个第VIII族和1个零族,周期表中有7个橫行,分为7个周期,故A正确;
B.元素周期中,原子最外电子层只有2个电子的元素,为He、碱土金属(ⅡA)或某些过渡金属元素,可能为金属元素,也可能为非金属元素,故B正确;
C.在元素周期表中位于金属元素和非金属元素交界处的元素具有半导体的性质,所以在元素周期表中位于金属元素和非金属元素交界处最容易找到半导体材料,故C错误;
D.从ⅢB族到ⅡB族10个纵行均为过渡元素,过渡元素全部为金属元素,故D正确.
故选C.
点评 本题考查元素周期表的结构及应用,把握元素周期表的结构为解答的关键,注意常见元素的位置及可能元素分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.在一定温度下的恒容密闭容器中,反应A(s)+2B(g)?C(g)+D(g),反应已达到平衡的标志是( )
| A. | 反应混合物中各组分的浓度相等 | B. | 混合气体的密度不再改变 | ||
| C. | 混合气体的压强不再变化 | D. | 两种物质C、D的反应速率之比为1:1 |
4.下列图示与对应的叙述相符的是( )
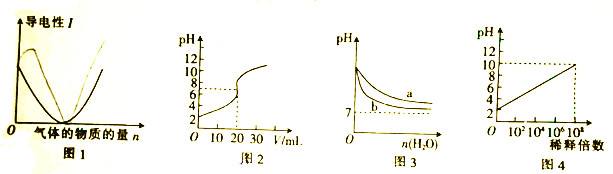

| A. | 图1可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 | |
| B. | 图2所示实验为常温下用0.01mol•L-1的HCl溶液滴定20mL0.01mol•L-1的NaOH溶液 | |
| C. | 图2可表示常温下pH相同的NaOH溶液与氨水稀释过程的pH变化,其中曲线b是氨水的pH变化 | |
| D. | 图4可以表示常温下pH=2的HCl溶液加水稀释倍数与pH的变化关系 |
16.为提纯如表物质(括号内为杂质)选用的试剂和分离方法都正确的是( )
| 物质 | 试剂 | 分离方法 | |
| ① | KNO3(NaCl) | 蒸馏水 | 降温结晶 |
| ② | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
| ③ | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
| ④ | Cl2(HCl) | 饱和NaCl溶液 | 洗气 |
| A. | ①③ | B. | ①④ | C. | 只有 ④ | D. | ③④ |
3.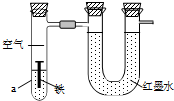 如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
 如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )
如图用来研究钢铁制品的腐蚀,装置的气密性良好,且开始时U形管两端的红墨水液面相平.一段时间后能观察到铁钉生锈.下列说法不正确的是( )| A. | 铁钉表面发生的反应为Fe-3e-=Fe3+ | |
| B. | 若液体a为稀盐酸,则U形管液面右高左低 | |
| C. | 若液体a为食盐水,则U形管液面左高右低 | |
| D. | 若液体a为食用油,则铁钉生锈速率较慢 |
13.下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A. | 都具有吸水性 | |
| B. | 露置于空气中都能形成白雾 | |
| C. | 露置于空气中,溶液浓度均降低 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
20.下列制取蒸馏水的实验装置与操作的说法中,不正确的是( )
| A. | 可用过滤的方法制取蒸馏水 | |
| B. | 冷凝器中的水流方向是从下口进入,上口排出 | |
| C. | 实验中需要在蒸馏烧瓶中加入几片碎瓷片或沸石 | |
| D. | 给蒸馏烧瓶加热时要垫上石棉网 |
17.下列描述正确的是( )
| A. | 氯水的标签上应标注: | B. | O2-的结构示意图: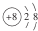 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | BeCl2的电子式: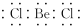 |
18.如图图象分别表示有关反应的反应过程与能量变化的关系:据此判断下列说法正确的是( )
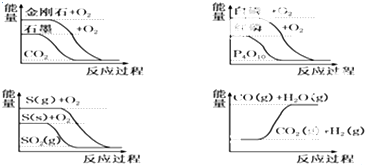

| A. | S(g)+O2(g)=SO2(g)△H1,S(s)+O2(g)=SO2(g)△H2,则△H1>△H2 | |
| B. | 白磷比红磷稳定 | |
| C. | 石墨转变为金刚石是吸热反应 | |
| D. | CO(g)+H2O(g)=CO2(g)+H2(g)△H>0 |