题目内容
【题目】海水经过晒盐后得到粗盐和苦卤,粗盐中除含有Ca2+,Mg2+,SO42﹣等可溶性杂质外,还含有泥沙等不溶性杂质,食用的精盐是用粗盐提纯得到,流程如图所示:
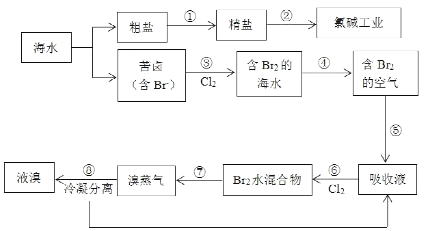
(1)为了除去粗盐中的Ca2+,Mg2+,SO42﹣,采取以下措施:
a.粗盐中含有的 Ca2+、Mg2+,精制过程中为除去这两种离子,发生的离子反应方程式分别为:_____,_____。
b.若粗盐中SO42﹣含量较高,必须添加钡试剂除去SO42﹣,该钡试剂可以是_____
A.Ba(OH)2
B.Ba(NO3)2
C.BaCl2
D.BaSO4
滴加钡试剂时,需注意(滴加试剂的先后顺序):_____。
(2)分离出粗盐后的苦卤还可用于溴元素的提取,在实验室中如何验证苦卤液中含有 Br﹣:_____。
(3)在苦卤提溴的过程中,第⑤步骤中可用亚硫酸钠溶液来吸收,则所发生的离子反应方程式为:_____,步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度 相差很大的特点进行分离。若在实验室分离上述混合物的分离仪器的名称是_____,分离时液 溴从分离器的_____(填“上口”或“下口”)排出。
【答案】Ca2++CO32﹣═CaCO3↓ Mg2++2OH﹣═Mg(OH)
2↓ AC 钡试剂加在 Na2CO3试剂之前 取样,向其中滴加新制氯水,振荡,向其中加入CCl4 溶液,振荡后溶液分层,下层溶液呈橙红色,则原试剂中含有Br﹣; SO32﹣+Br2+H2O=SO42﹣+2Br﹣+2H+ 分液漏斗 下口
【解析】
(1)a.Ca2+、Mg2+等杂质可与碳酸钠、NaOH反应转化为沉淀;
b.SO42﹣可以用含有钡离子的盐来处理,但是不能引入新杂质;SO42﹣、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,过滤后,滤液再加盐酸除去剩余食物碳酸钠和氢氧化钠;
(2)溴离子可被氯气氧化生成单质,溶于四氯化碳呈橙红色,据此分析;
(3)溴具有氧化性,可氧化亚硫酸根离子为硫酸根离子,据此写出离子方程式;由于液溴和溴水密度相差较大,溶液分层,可采用分液法进行分离。
(1)a.Ca2+、Mg2+等杂质分别与碳酸钠、NaOH反应转化为沉淀,离子反应分别为Ca2++CO32﹣═CaCO3↓、Mg2++2OH﹣═Mg(OH)2↓;
故答案为:Ca2++CO32﹣═CaCO3↓、Mg2++2OH﹣═Mg(OH)2↓;
b.添加钡试剂除去SO42﹣,注意不能引入新的杂质,选Ba(NO3)2会引入杂质硝酸根离子,所以该钡试剂不能选用,硫酸钡本身为沉淀,该钡试剂不能选用,所以AC符合;SO42﹣、Ca2+、Mg2+等分别与BaCl2溶液、Na2CO3溶液、NaOH溶液反应生成沉淀,可再通过过滤除去,Na2CO3溶液能除去过量的BaCl2溶液,则加入试剂应满足钡试剂加在 Na2CO3试剂之前;
故答案为:AC;钡试剂加在 Na2CO3试剂之前;
(2)溴离子可被氯气氧化生成单质,溶于四氯化碳呈橙红色,则可取样,向其中滴加新制氯水,振荡,向其中加入CCl4 溶液,振荡后溶液分层,下层溶液呈橙红色,则原试剂中含有 Br﹣;
故答案为:取样,向其中滴加新制氯水,振荡,向其中加入CCl4 溶液,振荡后溶液分层,下层溶液呈橙红色,则原 试剂中含有 Br﹣;
(3)溴具有氧化性,可氧化亚硫酸根离子,反应的离子方程式为SO32﹣+Br2+H2O=SO42﹣+2Br﹣+2H+,由于液溴和溴水密度相差较大,溶液分层,可用分液漏斗分离,溴在下层,应从下口分离,
故答案为:SO32﹣+Br2+H2O=SO42﹣+2Br﹣+2H+;分液漏斗;下口。