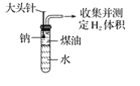
题目内容
【题目】下列电离方程式正确的是
A. NaHCO3水溶液中:NaHCO3 = Na++HCO3-
B. KHSO4水溶液中:KHSO4=K++HSO4-
C. Ca(OH)2在水中:Ca(OH)2![]() Ca2++2OH-
Ca2++2OH-
D. HClO=H++ClO-
【答案】A
【解析】
A.碳酸氢根离子是多元弱酸的酸式根离子,不能拆,NaHCO3的电离方程式为:NaHCO3=Na++HCO3-,故A正确;
B.KHSO4是强电解质,溶于水完全电离,电离方程式为:KHSO4=K++SO42-+H+,故B错误;
C.Ca(OH)2属于强电解质,在水中完全电离,电离方程式为:Ca(OH)2=Ca2++2OH-,故C错误;
D.HClO是弱酸,属于弱电解质,在水中部分发生电离,电离方程式为:HClO![]() H++ClO-,故D错误。
H++ClO-,故D错误。
故选A。

练习册系列答案
相关题目
【题目】有关下列四个常用电化学装置的叙述中,正确的是
|
|
|
|
图Ⅰ碱性锌锰电池 | 图Ⅱ铅-硫酸蓄电池 | 图Ⅲ电解精炼铜 | 图Ⅳ银锌纽扣电池 |
A. 图Ⅰ所示电池中,MnO2的作用是催化剂
B. 图Ⅱ所示电池放电过程中,硫酸浓度不断增大
C. 图Ⅲ所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图Ⅳ所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
【题目】某同学研究浓度对化学平衡的影响,下列说法正确的是
已知: | |
步骤:
| 现象: 待试管b中颜色不变后与试管a比较,溶液颜色变浅。 滴加浓硫酸,试管c温度略有升高,溶液颜色与试管a相比,变深。 |
A. 该反应是一个氧化还原反应
B. 待试管b中溶液颜色不变的目的是使![]() 完全反应
完全反应
C. 该实验不能证明减小生成物浓度,平衡正向移动
D. 试管c中的现象说明影响平衡的主要因素是温度