题目内容
下列叙述中正确的是( )?A.氯化钠溶液中,氯化钠在电流的作用下电离成钠离子或氯离子?
B.溶于水后能电离出氢离子的化合物都是酸?
C.硫酸钡难溶于水,但硫酸钡是强电解质?
D.SO2溶于水后部分电离,故二氧化硫属于弱电解质?
解析:A项不正确,氯化钠溶液中,氯化钠在水分子的作用下电离成钠离子或氯离子;B项不正确,溶于水后能电离出的阳离子全部是氢离子的化合物称为酸;C项强弱电解质的定义与物质的溶解性无关,仅与在水中的电离程度有关,硫酸钡难溶于水,但硫酸钡溶解的部分能完全电离是强电解质;D项SO2溶于水后生成的H2SO3是弱电解质,能电离,但SO2本身不能电离,是非电解质,D不正确。?
答案:C

练习册系列答案
相关题目
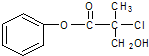 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


