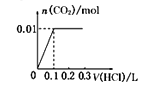题目内容
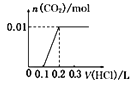
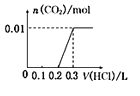
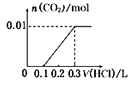
【题目】已知在酸性条件下有以下反应关系:KBrO3能将KI氧化成I2; Br2能将I﹣氧化为I2 . IO3﹣也能将Br﹣氧化为Br2 , 其本身被还原为I2 . 现向含有1mol KI的硫酸溶液中加入含amol KBrO3溶液,a的取值不同,所得产物也不同.下列判断正确是( )
编号 | a的取值范围 | 产物的化学式(或离子符号) |
① | a≤ | I2Br﹣ |
② |
| I2Br﹣Br2 |
③ |
| I2 IO3﹣ Br2 |
④ | a≥ | IO3﹣ Br2 |
A.①③④
B.②③④
C.①②③④
D.①④
【答案】C
【解析】解:当a≤ ![]() 时,KBrO3不足,反应生成I2、Br﹣ , 反应方程式为:6KI+KBrO3+3H2SO4=3I2+KBr+3K2SO4+3H2O;
时,KBrO3不足,反应生成I2、Br﹣ , 反应方程式为:6KI+KBrO3+3H2SO4=3I2+KBr+3K2SO4+3H2O;
当a= ![]() 时,二者反应生成I2、Br2 , 反应方程式为:10KI+2KBrO3+6H2SO4=5I2+Br2+6K2SO4+6H2O;
时,二者反应生成I2、Br2 , 反应方程式为:10KI+2KBrO3+6H2SO4=5I2+Br2+6K2SO4+6H2O;
当 ![]() <a<
<a< ![]() 时:反应产物为:I2、Br﹣、Br2 , 发生以上两个反应;
时:反应产物为:I2、Br﹣、Br2 , 发生以上两个反应;
当a≥ ![]() 时,KBrO3足量,发生反应为:5KI+6KBrO3+3H2SO4=5KIO3+3Br2+3K2SO4+3H2O,所以反应产物为:IO3﹣、Br2;
时,KBrO3足量,发生反应为:5KI+6KBrO3+3H2SO4=5KIO3+3Br2+3K2SO4+3H2O,所以反应产物为:IO3﹣、Br2;
当 ![]() <a<
<a< ![]() 时,反应按照C、E中的反应进行,反应产物为:I2、IO3﹣、Br2 , 则有:
时,反应按照C、E中的反应进行,反应产物为:I2、IO3﹣、Br2 , 则有:
编号 | a的取值范围 | 产物的化学式或(离子符号) |
① | a≤ | I2 , Br﹣ |
② |
| I2、Br﹣、Br2 |
a= | I2、Br2 | |
③ |
| I2、IO3﹣、Br2 |
④ | a≥ | IO3﹣、Br2 |
故选C.

 课堂全解字词句段篇章系列答案
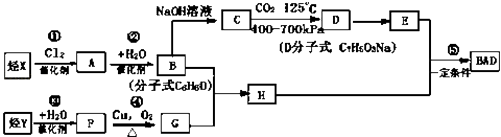
课堂全解字词句段篇章系列答案【题目】工业上由N2、H2合成NH3 . 制备H2需经多步完成,其中“水煤气(CO、H2)变换”是纯化H2的关键一步.
(1)水煤气变换:CO(g)+H2O(g)CO2(g)+H2(g),平衡常数K随温度变化如表:
温度/℃ | 200 | 300 | 400 |
K | 290 | 39 | 11.7 |
①下列分析正确的是 .
a.水煤气变换反应的△H<0
b.增大压强,可以提高CO的平衡转化率
c.增大水蒸气浓度,可以同时增大CO的平衡转化率和反应速率
②以氨水为吸收剂脱除CO2 . 当其失去吸收能力时,通过加热使吸收剂再生.用化学方程式表示“吸收”、“再生”两个过程: .
(2)Fe3O4是水煤气变换反应的常用催化剂,经CO、H2还原Fe2O3制备.两次实验结果如表:
实验Ⅰ | 实验Ⅱ | |
通入气体 | CO、H2 | CO、H2、H2O(g) |
固体产物 | Fe3O4、Fe | Fe3O4 |
结合化学方程式解释H2O(g)的作用: .
(3)2016年我国某科研团队利用透氧膜,一步即获得N2、H2 , 工作原理如图所示.(空气中N2与O2的物质的量之比按4:1计) 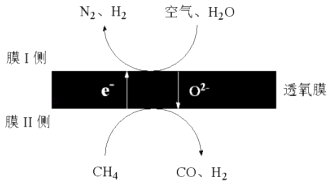
①起还原作用的物质是 .
②膜Ⅰ侧发生的电极反应式是 .
③膜Ⅰ侧所得气体 ![]() =3,CH4、H2O、O2反应的化学方程式是 .
=3,CH4、H2O、O2反应的化学方程式是 .
【题目】元素周期表是学习和研究化学的重要工具。短周期元素甲~戊在元素周期表中的相对位置如表所示,下列判断正确的是
甲 | 乙 | 丙 |
丁 | 戊 |
A. 原子半径:丙>甲B. 原子核外电子层数:戊<丁
C. 原子核外最外层电子数:丙>戊>丁D. 元素的最高价氧化物的水化物的酸性:戊<丁