题目内容
【题目】(实验1)探究草酸的制备:
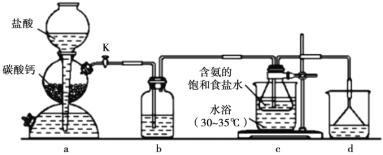
实验室用硝酸氧化淀粉(C6H12O6)水解液法(水浴加热)制备草酸,其反应为:C6H12O6+12HNO3 = 3H2C2O4+9NO2↑+3NO↑+9H2O ,装置如图所示:
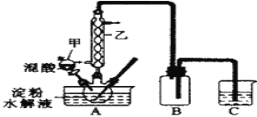
(1)仪器乙的名称为:_________,其接通冷水与水浴加热三颈瓶的先后顺序是:________
(2)烧杯C中盛放的溶液是___________,装置的B作用是______________
(实验2)探究草酸的不稳定性:
已知:草酸晶体(H2C2O4·2H2O)无色,易溶于水,熔点为101℃,受热易脱水、升华,170℃以上分解产生H2O、CO和CO2,其酸性比碳酸强,其钙盐难溶于水。
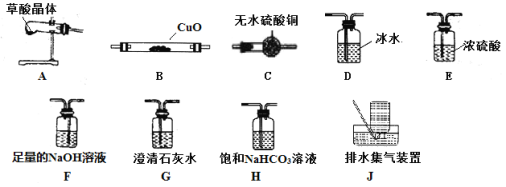
(3)请选取以上的装置证明草酸晶体分解的产物(可重复使用,加热装置和连接装置已略去)。仪器装置连接顺序为:A→_______→______→______→_______→E→B→G→_______。
(4)若实验结束后测得B管质量减轻4.8g,则至少需分解草酸晶体的质量为_________g
【答案】球形冷凝管 先通冷水,后水浴加热三颈瓶 NaOH溶液 防止倒吸 C D G F J 37.8g
【解析】
(1)仪器乙的名称为球形冷凝管,冷凝管是不耐热的仪器,加热前应先通冷水,以防冷凝管炸裂。
(2)烧杯C中盛放的溶液应能够吸收尾气,装置B的作用是防止倒吸。
(3)在确定仪器装置连接顺序时,应考虑先检验水蒸气,再检验CO2,最后检验CO。在检验CO2前,需考虑草酸易升华,所以应先去除草酸,再检验CO2;在检验CO前,需先除尽CO2,最后还应处理尾气。
(4) H2C2O4·2H2O![]() 3H2O+CO↑+CO2↑,CO+CuO
3H2O+CO↑+CO2↑,CO+CuO![]() Cu+CO2,B管减轻的质量就是参加反应的O原子的质量。从而得出关系式H2C2O4·2H2O—CO—O,由O原子的质量便可求出至少需分解草酸晶体的质量。
Cu+CO2,B管减轻的质量就是参加反应的O原子的质量。从而得出关系式H2C2O4·2H2O—CO—O,由O原子的质量便可求出至少需分解草酸晶体的质量。
(1)仪器乙的名称为球形冷凝管,冷凝管是不耐热的仪器,加热前应先通冷水,以防冷凝管炸裂,所以应先通冷水,后水浴加热三颈瓶。答案为:球形冷凝管;先通冷水,后水浴加热三颈瓶;
(2)烧杯C中盛放的溶液应能够吸收氮的氧化物的NaOH溶液,装置B的作用是防止倒吸。答案为:NaOH溶液;防止倒吸;
(3)在确定仪器装置连接顺序时,应考虑先检验水蒸气,再检验CO2,最后检验CO。在检验CO2前,需考虑草酸易升华,所以应先去除草酸,再检验CO2;在检验CO前,需先除尽CO2,最后还应处理尾气。从而得出仪器装置连接顺序为:A→C→D→G→F→E→B→G→J。答案为:C;D;G;F;J;
(4) H2C2O4·2H2O![]() 3H2O+CO↑+CO2↑,CO+CuO
3H2O+CO↑+CO2↑,CO+CuO![]() Cu+CO2,B管减轻的质量就是参加反应的O原子的质量。从而得出关系式H2C2O4·2H2O—CO—O,n(O)=
Cu+CO2,B管减轻的质量就是参加反应的O原子的质量。从而得出关系式H2C2O4·2H2O—CO—O,n(O)=![]() =0.3mol,则n(H2C2O4·2H2O)= n(O)=0.3mol,m(H2C2O4·2H2O)= 0.3mol×126g/mol=37.8g。答案为:37.8g。
=0.3mol,则n(H2C2O4·2H2O)= n(O)=0.3mol,m(H2C2O4·2H2O)= 0.3mol×126g/mol=37.8g。答案为:37.8g。

【题目】金属钛(Ti)被称为21世纪金属,在航海、航空、记忆和涂料方面应用广泛,TiO2是一种优良的光催化剂。20世纪科学家尝试用多种方法将金红石(TiO2)还原,发现金红石直接氯化是冶炼钛的关键。
步骤:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH=+1493kJmol-1,ΔS=+61JK-1mol-1
该反应发生温度高达2170℃,能耗大,对设备和生产要求几乎达到苛刻程度。目前科学家采用金红石加碳氯化方法,在较温和条件下成功制取TiCl4,为人类快速迈进钛合金时代做出了巨大贡献。金红石加碳氯化的主要反应如下:
反应Ⅰ:TiO2(s)+2Cl2(g) +C(s)![]() TiCl4(g)+CO2(g) ΔH1,ΔS1=+64JK-1mol-1
TiCl4(g)+CO2(g) ΔH1,ΔS1=+64JK-1mol-1
反应Ⅱ:TiO2(s)+2Cl2(g) +2C(s)![]() TiCl4(g)+2CO(g) ΔH2,△S2
TiCl4(g)+2CO(g) ΔH2,△S2
已知:①C(s)+O2(g)=CO2(g) ΔH=-394.3kJmol-1
②2C(s)+O2(g)=2CO(g) ΔH=-222.3kJmol-1
请回答:
(1)反应Ⅰ的ΔH1=__kJmol-1。
(2)对于气体参加的反应,表示平衡常数KP时,用气体组分B的平衡压强P(B)代替该气体物质的量浓度c(B),则反应Ⅰ的KP=__(用表达式表示)。
(3)在常温、常压、光照条件下,N2在催化剂TiO2表面与H2O发生反应,2N2(g)+6H2O(1)=4NH3(g)+3O2(g) ΔH=+1530.4kJmol-1
进一步研究相同条件下NH3生成量与温度的关系,部分实验数据见表:
实验组别 | 1 | 2 | 3 | 4 |
T/K | 303 | 313 | 323 | 353 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
O2生成量/(10-6mol) | 3.6 | 4.4 | 4.5 | 1.5 |
反应时间/h | 3 | 3 | 3 | 3 |
容器体积/L | 2 | 2 | 2 | 2 |
①请在如图中画出上述反应在“有催化剂”与“无催化剂”两种情况下反应过程中体系能量随反应过程的变化趋势示意图(图中标明必要的文字说明)。___
②根据表中数据,在303K时,在3h内用氮气表示其平均反应速率为___molL-1h-1。判断组别4中反应是否达到平衡状态___(填“是”或“否”),并说明理由___。