��Ŀ����
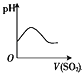
����Ŀ��I. ��֪��ѧ��ӦA2(g)��B2(g)===2AB(g)�������仯��ͼ��ʾ��������������ȷ����

(1)a��b�ֱ��������˼��_______________��___________________��
(2)�÷�Ӧ��H_______________________
��������ͼװ�ÿ���֤ͬ����Ԫ�طǽ����Եı仯���ɡ�

��3������A������Ϊ________________�������D������Ϊ___________________��
��4����Ҫ֤���ǽ����ԣ�Cl��I��C��Ϊ�������⻯�ػ����Һ��B��װ��KMnO4���壬��A���Լ�Ϊ________���۲쵽C����Һ____________ (������)������֤�����ӻ��������Ĺ۵㿼�ǣ���װ��ȱ�� __________��
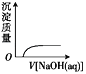
��5����Ҫ֤���ǽ����ԣ�S>C��Si������A��__________B�м�_________��C�м�__________��д��C�з�Ӧ�Ļ�ѧ����ʽ______________________________
���𰸡��ɼ��������յ����� �¼��γɷų������� ��H����(a��b)kJ/mol ��Һ©�� ��ֹ���� Ũ���� ��Һ��Ϊ��ɫ �ж�����������������Ⱦ������ȱβ������װ�ã� ϡ���� Na2CO3 Na2SiO3��Һ Na2SiO3 +CO2 +H2O = Na2CO3 +H2SiO3��
��������
I.���÷�Ӧ�������������������������Ĵ�С���жϸ÷�Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ��ע���ܵĶ��壻
II.ӦŪ���ʵ��Ŀ�ĺ�ʵ��ԭ����Ȼ�����з�����
I.��1������ͼ��a��ʾ���Ƕϼ����յ�������������Ӧ�Ļ�ܣ�b���������γɻ�ѧ��ʱ�ų������������淴Ӧ�Ļ�ܣ�
��2����Ӧ��������С������������������÷�ӦΪ���ȷ�Ӧ����H>0����H=+(a��b)kJ��mol��1��
II.��3������AΪ��Һ©��������ܵ������Ƿ�ֹ������
��4����֤Cl�ķǽ�����ǿ��I������Cl2��2I��=2Cl����I2�������ƿ��Ŀ�����Ʊ�Cl2������Һ©����ʢ�ŵ���Ũ���C������I2����Һ��Ϊ��ɫ��Cl2�ж�����˱�װ��ȱ��β������װ�ã�
��5��֤������Ԫ�صķǽ����ԣ�ԭ�����ж�����Ԫ������������Ӧˮ��������ԣ�����Խǿ����ǽ�����Խǿ����A��ʢ��ϡ���ᣬB��ʢ��Na2CO3��C��ʢ�Ź����ƣ�B�г������ݣ�˵��S�ķǽ�����ǿ��C��C�г��ְ�ɫ������˵��C�ķǽ�����ǿ��Si��C�з�����ѧ����ʽΪNa2SiO3��CO2��H2O=Na2CO3��H2SiO3����