题目内容
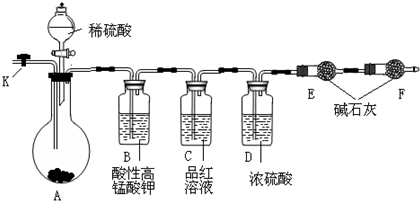
为测定Na2CO3与Na2SO3混合物中各组分的含量,欲取样品m g以图所示装置进行实验,已知仪器C中装有品红溶液.(铁架台、铁夹等仪器未在图中画出)
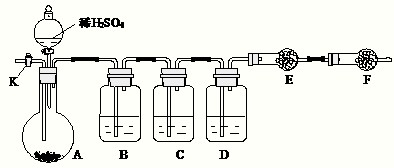
(1)将仪器连接好以后,必须进行的第一步操作是
(2)此实验还必须用到的最重要的仪器是
(3)实验室中备有以下常用试剂:
a.浓硫酸 b.品红溶液 c.酸性高锰酸钾溶液 d.饱和碳酸氢钠溶液 e.氢氧化钠溶液
f.无水硫酸铜 g.碱石灰 h.五氧化二磷 i.无水氯化钙
请将下列容器中应盛放的试剂序号填入相应空格:B中
(4)实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的空气.这样做的目的是
所通空气应先经过
(5)若要提高实验的准确性,还应在

(1)将仪器连接好以后,必须进行的第一步操作是
检验装置的气密性
检验装置的气密性
.(2)此实验还必须用到的最重要的仪器是
托盘天平
托盘天平
;仪器F的作用是防止空气中的水蒸气、二氧化碳进入E装置中
防止空气中的水蒸气、二氧化碳进入E装置中
.(3)实验室中备有以下常用试剂:
a.浓硫酸 b.品红溶液 c.酸性高锰酸钾溶液 d.饱和碳酸氢钠溶液 e.氢氧化钠溶液
f.无水硫酸铜 g.碱石灰 h.五氧化二磷 i.无水氯化钙
请将下列容器中应盛放的试剂序号填入相应空格:B中
c
c
,D中a
a
,E中g
g
.(4)实验过程中,当仪器A内的固体反应完全后,需打开活塞K,向A中通入大量的空气.这样做的目的是
使生成的二氧化碳能够全部装置E中药品吸收
使生成的二氧化碳能够全部装置E中药品吸收
.所通空气应先经过
e或g
e或g
试剂(填序号)处理,否则可能引起Na2SO3 含量的测量结果比实际值偏低
偏低
(填“偏高”、“偏低”或“无影响”).(5)若要提高实验的准确性,还应在
D与E
D与E
之间增加装有i
i
(填序号)的球形干燥管装置.分析:由装置图可知,实验原理为:混合物中加入硫酸,转化为二氧化硫、二氧化碳,除去反应生成的二氧化硫,利用E装置的增重确定生成的二氧化碳的质量,根据二氧化碳的质量计算混合物中碳酸钠的质量,进而计算各组分的质量分数.
(1)由于需要测定二氧化碳的质量,整套装置应气密性良好,故实验之前应检验装置的气密性;
(2)实验测定二氧化碳的质量,进而计算碳酸钠的质量,要计算质量分数,需要知道样品的总质量,故应需要用托盘天平称量样品的质量;
利用E装置的增重确定生成的二氧化碳的质量,故F装置目的是防止空气中的水蒸气、二氧化碳进入E装置中,影响测量结果;
(3)实验原理是除去反应生成的二氧化硫,利用E装置的增重确定生成的二氧化碳的质量,根据二氧化碳的质量计算混合物中碳酸钠的质量,故进入装置E中的二氧化碳要干燥、不含二氧化硫,故装置B的作用是除去气体中的二氧化硫,试剂保证吸收二氧化硫,不能吸收二氧化碳且不能生成二氧化碳,装置C的作用是具有二氧化硫是否除尽,装置D的作用是干燥气体;
(4)装置内会残留部分二氧化碳,应使二氧化碳区别被装置E中药品吸收,故通入大量的空气目的是排尽装置内的二氧化碳,使生成的二氧化碳能够全部装置E中药品吸收.由于空气中含有二氧化碳,应先除去空气中的二氧化碳.若不除去空气中的二氧化碳,导致测定二氧化碳的质量增大,计算所得碳酸钠的质量增大,引起测定的Na2S03质量减小;
(5)装置E吸收二氧化碳后会生成水,防止装置D的浓硫酸吸收影响二氧化碳的质量测定.
(1)由于需要测定二氧化碳的质量,整套装置应气密性良好,故实验之前应检验装置的气密性;
(2)实验测定二氧化碳的质量,进而计算碳酸钠的质量,要计算质量分数,需要知道样品的总质量,故应需要用托盘天平称量样品的质量;
利用E装置的增重确定生成的二氧化碳的质量,故F装置目的是防止空气中的水蒸气、二氧化碳进入E装置中,影响测量结果;
(3)实验原理是除去反应生成的二氧化硫,利用E装置的增重确定生成的二氧化碳的质量,根据二氧化碳的质量计算混合物中碳酸钠的质量,故进入装置E中的二氧化碳要干燥、不含二氧化硫,故装置B的作用是除去气体中的二氧化硫,试剂保证吸收二氧化硫,不能吸收二氧化碳且不能生成二氧化碳,装置C的作用是具有二氧化硫是否除尽,装置D的作用是干燥气体;
(4)装置内会残留部分二氧化碳,应使二氧化碳区别被装置E中药品吸收,故通入大量的空气目的是排尽装置内的二氧化碳,使生成的二氧化碳能够全部装置E中药品吸收.由于空气中含有二氧化碳,应先除去空气中的二氧化碳.若不除去空气中的二氧化碳,导致测定二氧化碳的质量增大,计算所得碳酸钠的质量增大,引起测定的Na2S03质量减小;
(5)装置E吸收二氧化碳后会生成水,防止装置D的浓硫酸吸收影响二氧化碳的质量测定.
解答:解:由装置图可知,实验原理为:混合物中加入硫酸,转化为二氧化硫、二氧化碳,除去反应生成的二氧化硫,利用E装置的增重确定生成的二氧化碳的质量,根据二氧化碳的质量计算混合物中碳酸钠的质量,进而计算各组分的质量分数.
(1)由于需要测定二氧化碳的质量,整套装置应气密性良好,故实验之前应检验装置的气密性;
故答案为:检验装置的气密性;
(2)实验测定二氧化碳的质量,进而计算碳酸钠的质量,要计算质量分数,需要知道样品的总质量,故应需要用托盘天平称量样品的质量;
利用E装置的增重确定生成的二氧化碳的质量,故F装置目的是防止空气中的水蒸气、二氧化碳进入E装置中,影响测量结果;
故答案为:托盘天平;防止空气中的水蒸气、二氧化碳进入E装置中;
(3)进入装置E中的二氧化碳要干燥、不含二氧化硫,故装置B的作用是除去气体中的二氧化硫,试剂保证吸收二氧化硫,不能吸收二氧化碳且不能生成二氧化碳,故选择c(酸性高锰酸钾溶液);
装置C的作用是具有二氧化硫是否除尽,装置D的作用是干燥气体,选择试剂为a(浓硫酸);
E装置的作用是吸收生成的二氧化碳,确定二氧化碳的质量,故可以选择g(碱石灰);
故答案为:c;a;g;
(4)装置内会残留部分二氧化碳,应使二氧化碳区别被装置E中药品吸收,故通入大量的空气目的是排尽装置内的二氧化碳,使生成的二氧化碳能够全部装置E中药品吸收.
由于空气中含有二氧化碳,应先除去空气中的二氧化碳,若不除去空气中的二氧化碳,导致测定二氧化碳的质量增大,计算所得碳酸钠的质量增大,引起测定的a2S03质量减小,导致Na2SO3含量偏低,可以使空气先通过氢氧化钠溶液或碱石灰除去含有的二氧化碳;
故答案为:使生成的二氧化碳能够全部装置E中药品吸收;e或g;偏低;
(5)装置E吸收二氧化碳后会生成水,防止装置D的浓硫酸吸收影响二氧化碳的质量测定,故在在D与E之间之间增加装有 氯化钙的球形干燥管装置;
故答案为:在D与E,i.
(1)由于需要测定二氧化碳的质量,整套装置应气密性良好,故实验之前应检验装置的气密性;
故答案为:检验装置的气密性;
(2)实验测定二氧化碳的质量,进而计算碳酸钠的质量,要计算质量分数,需要知道样品的总质量,故应需要用托盘天平称量样品的质量;
利用E装置的增重确定生成的二氧化碳的质量,故F装置目的是防止空气中的水蒸气、二氧化碳进入E装置中,影响测量结果;
故答案为:托盘天平;防止空气中的水蒸气、二氧化碳进入E装置中;
(3)进入装置E中的二氧化碳要干燥、不含二氧化硫,故装置B的作用是除去气体中的二氧化硫,试剂保证吸收二氧化硫,不能吸收二氧化碳且不能生成二氧化碳,故选择c(酸性高锰酸钾溶液);
装置C的作用是具有二氧化硫是否除尽,装置D的作用是干燥气体,选择试剂为a(浓硫酸);
E装置的作用是吸收生成的二氧化碳,确定二氧化碳的质量,故可以选择g(碱石灰);
故答案为:c;a;g;
(4)装置内会残留部分二氧化碳,应使二氧化碳区别被装置E中药品吸收,故通入大量的空气目的是排尽装置内的二氧化碳,使生成的二氧化碳能够全部装置E中药品吸收.
由于空气中含有二氧化碳,应先除去空气中的二氧化碳,若不除去空气中的二氧化碳,导致测定二氧化碳的质量增大,计算所得碳酸钠的质量增大,引起测定的a2S03质量减小,导致Na2SO3含量偏低,可以使空气先通过氢氧化钠溶液或碱石灰除去含有的二氧化碳;
故答案为:使生成的二氧化碳能够全部装置E中药品吸收;e或g;偏低;
(5)装置E吸收二氧化碳后会生成水,防止装置D的浓硫酸吸收影响二氧化碳的质量测定,故在在D与E之间之间增加装有 氯化钙的球形干燥管装置;
故答案为:在D与E,i.
点评:本题考查学生对实验原理的理解、物质组成的测定等,难度中等,理解原理是关键,需要学生具有扎实的基础知识与综合运用知识分析解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
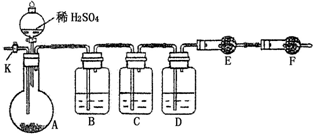
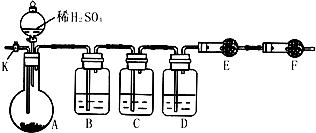 (2012?丹东模拟)为测定Na2CO3与Na2SO3混合物中各组分的含量,设计如下实验方案:
(2012?丹东模拟)为测定Na2CO3与Na2SO3混合物中各组分的含量,设计如下实验方案: