题目内容
能源材料已成为当今科学研究的热点.请回答下列问题:
(1)单质A的燃烧热大,可作燃料.已知A为短周期元素,其气态原子逐个失去1~4个电子所需能量(电离能)如表所示,某同学推断A的核外电子排布为:1s22s22p63s13p1,该电子排布式违背了 ;若该原子核外电子确有三层,则该元素位于周期表 族,写出A燃烧后形成的氧化物的电子式: .
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.继C60后,科学家又合成了Si60、N60,下列有关说法正确的是 (填序号).
a.C60、Si60、N60都属于新型化合物
b.C60、Si60、N60互为同分异构体
c.已知N60结构与C60相似,由于N-N键能小于N≡N,故N60的稳定性弱于N2
d.已知金刚石中C-C键长154pm,C60中C-C键长145~140pm,故C60熔点高于金刚石
(3)超导材料在节能、储能方面的应用.如图是超导材料元素在周期表中的分布,其中短周期元素中原子半径最大的是 (填元素符号),其原子最外层有 种运动状态不同的电子,写出其最高价氧化物对应水化物的电离方程式: .

(1)单质A的燃烧热大,可作燃料.已知A为短周期元素,其气态原子逐个失去1~4个电子所需能量(电离能)如表所示,某同学推断A的核外电子排布为:1s22s22p63s13p1,该电子排布式违背了
| I1 | I2 | I3 | I4 | … | |
| 电离能(kJ/mol) | 738 | 1451 | 7733 | 10540 | … |
a.C60、Si60、N60都属于新型化合物
b.C60、Si60、N60互为同分异构体
c.已知N60结构与C60相似,由于N-N键能小于N≡N,故N60的稳定性弱于N2
d.已知金刚石中C-C键长154pm,C60中C-C键长145~140pm,故C60熔点高于金刚石
(3)超导材料在节能、储能方面的应用.如图是超导材料元素在周期表中的分布,其中短周期元素中原子半径最大的是

分析:(1)A的核外电子排布违背能量最低原理;
该原子核外电子确有三层,A的核外电子排布应为:1s22s22p63s2,最外层电子数等于族序数;
其氧化物为MgO,属于离子化合物,由镁离子与氧离子构成;
(2)a.由两种或两种以上元素组成的纯净物为化合物;
b.同分异构体研究对象为化合物;
c.键能越小,化学键越不稳定;
d.金刚石属于原子晶体,C60属于分子晶体,原子晶体的熔点更高;
(3)同周期自左而右原子半径减小,电子层越多原子半径越大,故超导材料元素中短周期内原子半径最大为Al元素;
原子中没有运动状态相同的电子,核外有几个电子,就有几种运动状态不同的电子;
氢氧化铝是两性氢氧化物,存在酸式电离,电离出偏铝酸根与氢离子,存在碱式电离,电离出铝离子与氢氧根离子.
该原子核外电子确有三层,A的核外电子排布应为:1s22s22p63s2,最外层电子数等于族序数;
其氧化物为MgO,属于离子化合物,由镁离子与氧离子构成;
(2)a.由两种或两种以上元素组成的纯净物为化合物;
b.同分异构体研究对象为化合物;
c.键能越小,化学键越不稳定;
d.金刚石属于原子晶体,C60属于分子晶体,原子晶体的熔点更高;
(3)同周期自左而右原子半径减小,电子层越多原子半径越大,故超导材料元素中短周期内原子半径最大为Al元素;
原子中没有运动状态相同的电子,核外有几个电子,就有几种运动状态不同的电子;
氢氧化铝是两性氢氧化物,存在酸式电离,电离出偏铝酸根与氢离子,存在碱式电离,电离出铝离子与氢氧根离子.
解答:解:(1)A的核外电子排布违背能量最低原理;
该原子核外电子确有三层,A的核外电子排布应为:1s22s22p63s2,处于ⅡA族;
其氧化物为MgO,属于离子化合物,由镁离子与氧离子构成,电子式为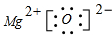 ,
,
故答案为:能量最低原理;ⅡA;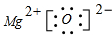 ;
;
(2)a.C60、Si60、N60都属于单质,故a错误;
b.同分异构体研究对象为化合物,C60、Si60、N60都属于单质,且分子式不相同,故b错误;
c.N-N键能小于N≡N,键能越小,化学键越不稳定,故N60的稳定性弱于N2,故c正确;
d.金刚石属于原子晶体,C60属于分子晶体,故金刚石的熔点高于C60,故d错误;
故答案为:c;
(3)同周期自左而右原子半径减小,电子层越多原子半径越大,故超导材料元素中短周期内原子半径最大为Al元素;
原子中没有运动状态相同的电子,Al原子最外层有3个电子,故最外层有3种运动状态不同的电子;
氢氧化铝是两性氢氧化物,存在酸式电离,电离出偏铝酸根与氢离子,存在碱式电离,电离出铝离子与氢氧根离子,电离方程式为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-,
故答案为:Al;3;H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
该原子核外电子确有三层,A的核外电子排布应为:1s22s22p63s2,处于ⅡA族;
其氧化物为MgO,属于离子化合物,由镁离子与氧离子构成,电子式为
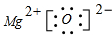 ,
,故答案为:能量最低原理;ⅡA;
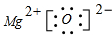 ;
;(2)a.C60、Si60、N60都属于单质,故a错误;
b.同分异构体研究对象为化合物,C60、Si60、N60都属于单质,且分子式不相同,故b错误;
c.N-N键能小于N≡N,键能越小,化学键越不稳定,故N60的稳定性弱于N2,故c正确;
d.金刚石属于原子晶体,C60属于分子晶体,故金刚石的熔点高于C60,故d错误;
故答案为:c;
(3)同周期自左而右原子半径减小,电子层越多原子半径越大,故超导材料元素中短周期内原子半径最大为Al元素;
原子中没有运动状态相同的电子,Al原子最外层有3个电子,故最外层有3种运动状态不同的电子;
氢氧化铝是两性氢氧化物,存在酸式电离,电离出偏铝酸根与氢离子,存在碱式电离,电离出铝离子与氢氧根离子,电离方程式为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-,
故答案为:Al;3;H++AlO2-+H2O?Al(OH)3?Al3++3OH-.
点评:本题考查结构性质位置关系、常用化学用语、化学基本概念、核外电子排布规律、物质结构与性质等,难度中等,注意对基础知识的理解掌握.

练习册系列答案
相关题目
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等
|
|
|
J |
|
|
|
|
|
|
|
R |
M的气态原子逐个失去1~ 4个电子所需能量(电离能)如下表所示,
|
|
I1 |
I2 |
I3 |
I4 |
…… |
|
电离能(kJ/mol) |
578 |
1817 |
2745 |
11578 |
…… |
(1)M的电子排布式为________;元素T在周期表中的位置为________。
(2)J和氢能形成多种化合物,其中分子成直线型的,且相对分子质量最小的物质的结构式为________。
(3)M和T形成的化合物在潮湿的空气中冒白雾,反应的化学方程式为_________________。
(4)由J、R形成的液态化合物JR2 0.2 mol在O2中完全燃烧,生成两种气态氧化物,298 K时放出热量215 kJ。该反应的热化学方程式为________。
(5)能源材料已成为当今科学研究的热点。氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。继C60后,科学家又合成了Si60、N60,下列有关说法正确的是_______(填序号)。
a. C60、Si60、N60都属于新型化合物
b. C60、Si60、N60互为同分异构体
c. 已知N60结构与C60相似,由于N-N键能小于N≡N,故N60的稳定性弱于N2
d. 已知金刚石中C-C键长154pm,C60中C-C键长145~140pm,故C60熔点高于金刚石
