题目内容
(2013?广东模拟)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: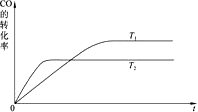
CO(g)+2H2(g)?CH3OH(g).
(1)该反应的平衡常数表达式为 K=
.
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H
②若容器容积不变,下列措施可增加甲醇产率的是
A.升高温度
B.将CH3OH(g)从体系中分离
C.使用合适的催化剂
D.充入He,使体系总压强增大
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1
③H2O(g)=H2O(l)△H=-c kJ?mol-1
则CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=
kJ?mol-1.

CO(g)+2H2(g)?CH3OH(g).
(1)该反应的平衡常数表达式为 K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| c(CH3OH) |
| c(CO)?c2(H2) |
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线.
①该反应的焓变△H
<
<
0(填“>”、“<”或“=”).②若容器容积不变,下列措施可增加甲醇产率的是
B
B
.A.升高温度
B.将CH3OH(g)从体系中分离
C.使用合适的催化剂
D.充入He,使体系总压强增大
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1
③H2O(g)=H2O(l)△H=-c kJ?mol-1
则CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=
| b-a-4c |
| 2 |
| b-a-4c |
| 2 |
分析:(1)平衡常数指平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;
(2)①根据先拐先平数值大原则,由图1可知,温度T1<T2,平衡时,温度越高CO的转化率越小,说明升高温度,平衡向逆反应移动,升高温度平衡向吸热反应移动,据此判断反应热;
②增加甲醇产率,应使化学平衡正向移动,结合平衡移动原理进行解答;
(3)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标方程式,反应热越乘以相应的系数并进行相应的计算.
(2)①根据先拐先平数值大原则,由图1可知,温度T1<T2,平衡时,温度越高CO的转化率越小,说明升高温度,平衡向逆反应移动,升高温度平衡向吸热反应移动,据此判断反应热;
②增加甲醇产率,应使化学平衡正向移动,结合平衡移动原理进行解答;
(3)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标方程式,反应热越乘以相应的系数并进行相应的计算.
解答:解:(1)可逆反应:CO(g)+2H2(g)?CH3OH(g)的平衡常数k=
,故答案为:
;
(2)①由图1可知,T2先达到平衡,温度T1<T2,平衡时,温度越高CO的转化率越小,说明升高温度,平衡向逆反应移动,升高温度平衡向吸热反应移动,故该反应正反应为放热反应,则△H<0,故答案为:<;
②增加甲醇产率,即化学平衡正向移动,则:
A.该反应为放热反应,升高温度,化学平衡逆向移动,甲醇产率降低,故A不符合;
B.将CH3OH(g)从体系中分离,平衡正向移动,可提高甲醇的产率,故B符合;
C.使用合适的催化剂,对化学平衡移动无影响,不能提高甲醇产率,故C不符合;
D.充入He,使体系总压强增大,反应体系中物质的浓度不变,平衡不移动,不能提高产率,故D不符合;
故答案为:B;
(3)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1,
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1,
③H2O(g)=H2O(l)△H=-c kJ?mol-1,
根据盖斯定律可知,则
可得CH3OH(l)+O2(g)=CO(g)+2H2O(l),则△H=
kJ/mol=
kJ/mol,
故答案为:
.
| c(CH3OH) |
| c(CO)?c2(H2) |
| c(CH3OH) |
| c(CO)?c2(H2) |
(2)①由图1可知,T2先达到平衡,温度T1<T2,平衡时,温度越高CO的转化率越小,说明升高温度,平衡向逆反应移动,升高温度平衡向吸热反应移动,故该反应正反应为放热反应,则△H<0,故答案为:<;
②增加甲醇产率,即化学平衡正向移动,则:
A.该反应为放热反应,升高温度,化学平衡逆向移动,甲醇产率降低,故A不符合;
B.将CH3OH(g)从体系中分离,平衡正向移动,可提高甲醇的产率,故B符合;
C.使用合适的催化剂,对化学平衡移动无影响,不能提高甲醇产率,故C不符合;
D.充入He,使体系总压强增大,反应体系中物质的浓度不变,平衡不移动,不能提高产率,故D不符合;
故答案为:B;
(3)①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-a kJ?mol-1,
②2CO(g)+O2(g)=2CO2(g)△H=-b kJ?mol-1,
③H2O(g)=H2O(l)△H=-c kJ?mol-1,
根据盖斯定律可知,则
| ①-②+③×4 |
| 2 |
| (-a)-(-b)+(-c)×4 |
| 2 |
| b-a-4c |
| 2 |
故答案为:
| b-a-4c |
| 2 |
点评:本题考查较为综合,涉及平衡常数、外界条件对平衡移动的影响、化学平衡图象、反应热的计算等问题,题目难度中等,本题注意利用盖斯定律进行反应热的有关计算.

练习册系列答案
相关题目

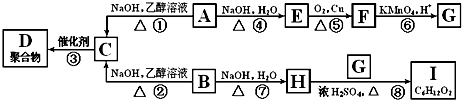





 +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl