题目内容
现有如下两个反应:
A.NaOH+HCl NaCl+H2O
NaCl+H2O
B.2FeCl3+Cu 2FeCl2+CuCl2
2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池:
A. ,B. (填“能”或“不能”);
(2)如果不能,说明其原因 ;
(3)如果可以,则写出正、负极材料及其电极反应式,电解质溶液名称:
负极材料 ,电极反应式 电解质溶液名称 ,正极材料 ,电极反应式 。
A.NaOH+HCl
 NaCl+H2O
NaCl+H2OB.2FeCl3+Cu
 2FeCl2+CuCl2
2FeCl2+CuCl2(1)根据两反应本质,判断能否设计成原电池:
A. ,B. (填“能”或“不能”);
(2)如果不能,说明其原因 ;
(3)如果可以,则写出正、负极材料及其电极反应式,电解质溶液名称:
负极材料 ,电极反应式 电解质溶液名称 ,正极材料 ,电极反应式 。
(10分) (1)不能;能 (2) A反应是非氧化还原反应
(3)铜;Cu- 2e-= Cu2+ ;氯化铁溶液;碳、铂、银;2Fe3+ + 2e-=2 Fe2+
(3)铜;Cu- 2e-= Cu2+ ;氯化铁溶液;碳、铂、银;2Fe3+ + 2e-=2 Fe2+
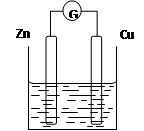
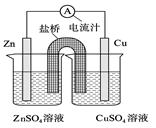
试题分析:原电池中有电子的定向运动,所以只有氧化还原反应才能设计成原电池。A是中和反应,不是氧化还原反应,不能设计成原电池。B是氧化还原反应,可以设计成原电池。由于原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。所以根据B中放热方程式可知,铜是还原剂,则铜作负极,正极的材料可以是碳或铂或银。铁离子得到电子,所以电解质容易应该是含有铁离子的可溶性盐溶液,因此可以性质氯化铁。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,有利于调动学生的学习兴趣,激发学生的学习积极性和创造性。该题的关键是明确原电池的工作原理,并能灵活运用即可。

练习册系列答案
相关题目