题目内容
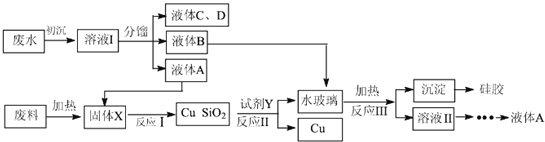
【题目】【2017景德镇二模】工业废渣、废水回收利用是重要研究课题.下面流程是生成食用香料正丁酸乙酯的工厂废水(含乙醇、正丁酸乙酯、正丁酸、乙酯和大量无机悬浮物)联合利用电子工业废料(含SiO2和Cu2(OH)2CO3)回收铜的工艺设计
回答下列问题:
(1)初沉加入的试剂是明矾.写出参与净水的离子的水解方程式 ;
(2)固体X的成分是 ,反应Ⅰ的化学方程式 ;
(3)试剂Y为 ;加快反应Ⅱ速率的措施有(任写一条) ;
(4)反应Ⅲ的离子方程式为 ;
(5)硅胶在生活与生产中用途广泛,写出一种用途 。
【答案】(1)Al3++3H2O![]() Al(OH)3+3H+ (2)CuO和SiO2;CH3CH2OH+CuO
Al(OH)3+3H+ (2)CuO和SiO2;CH3CH2OH+CuO![]() Cu+H2O+CH3CHO (3)氢氧化钠溶液 升高溶液的温度、增大氢氧化钠溶液浓度、增大固体接触面积等 (4)2CH3CH2CH2COOCH2CH3+SiO32﹣+2H2O=2CH3CH2CH2COO﹣+2CH3CH2OH+H2SiO3↓ (5)催化剂载体
Cu+H2O+CH3CHO (3)氢氧化钠溶液 升高溶液的温度、增大氢氧化钠溶液浓度、增大固体接触面积等 (4)2CH3CH2CH2COOCH2CH3+SiO32﹣+2H2O=2CH3CH2CH2COO﹣+2CH3CH2OH+H2SiO3↓ (5)催化剂载体
【解析】流程分析可知,废水(含乙醇、正丁酸乙酯、正丁酸、乙酯和大量无机悬浮物),废水积沉得到溶液Ⅰ分馏得到液体C、D,B为正丁酸乙酯,A为乙醇,CD为正丁酸、乙酯,反应Ⅲ为液体B为正丁酸乙酯和水玻璃溶液反应发生水解,生成丁酸钠,硅酸沉淀和乙醇,废料加热分解碱式碳酸铜分解生成氧化铜、二氧化碳和水,得到固体X为CuO、SiO2,其中氧化铜和液体A为乙醇加热反应生成铜,乙醛和水,得到Cu和SiO2和试剂Y发生反应得到硅酸钠溶液,说明是二氧化硅和碱发生的反应,Y为氢氧化钠溶液;
(1)明矾为硫酸铝钾,溶解后溶液中铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的主要,起到净水作用,反应的离子方程式为:Al3++3H2O![]() Al(OH)3+3H+;
Al(OH)3+3H+;
(2)上述分析可知固体X为氧化铜和二氧化硅,化学式为CuO和SiO2,乙醇和氧化铜加热反应生成铜和乙醛和水,反应的化学方程式为:CH3CH2OH+CuO![]() Cu+H2O+CH3CHO;
Cu+H2O+CH3CHO;
(3)上述分析可知试剂Y为氢氧化钠溶液,加快反应速率的措施可以利用升高溶液的温度、增大氢氧化钠溶液浓度、增大固体接触面积等;
(4)反应Ⅲ为正丁酸乙酯在水玻璃溶液中水解,结合流程图分析得到沉淀为硅酸,溶液Ⅱ为正丁酸钠和乙醇,蒸馏得到乙醇,反应的化学方程式为:2CH3CH2CH2COOCH2CH3+SiO32﹣+2H2O=2CH3CH2CH2COO﹣+2CH3CH2OH+H2SiO3↓;
(5)硅胶具有强力吸附能迅速有效地吸附密封包装内的水分、化学性质稳定、无毒无害的特点,可以做干燥剂、催化剂载体等。