题目内容
【题目】【2017浙江模拟】在烧瓶放20克蔗糖,依次加入少量水、20mL浓硫酸,蔗糖逐渐变黑,体积膨胀,形成疏松多孔的黑面包,烧瓶发烫,品红溶液颜色变淡.请回答:
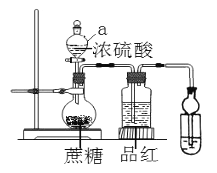
(1)仪器a的名称 ;
(2)小试管盛装试剂 ;
(3)下列说法不正确的是 ;
A.蔗糖变黑说明发生过程 C12H22O11→C+H2O
B.品红颜色变淡说明SO2有漂白性
C.上述实验体现浓硫酸的脱水性、吸水性和氧化性
D.将气体依次通过饱和碳酸氢钠溶液、澄清石灰水,石灰水变浑浊证明含有CO2.
【答案】(1) 分液漏斗 (2) NaOH或氨水 (3)D
【解析】在烧瓶放20克蔗糖,依次加入少量水、20mL浓硫酸,蔗糖逐渐变黑,浓硫酸具有脱水性,体积膨胀,形成疏松多孔的黑面包,是碳和浓硫酸加热反应生成二氧化碳、二氧化硫,烧瓶发烫反应放热,品红溶液颜色变淡,说明生成的二氧化硫具有漂白性,
(1)仪器a是添加溶液,控制液体流速和体积的仪器,为分液漏斗;
(2)生成的二氧化硫是污染性气体,不能排放到空气中,需要通过氢氧化钠溶液或氨水溶液吸收;
(3)A.蔗糖为碳氢氧化合物,浓分子式C12H22O11,硫酸具有脱水性,氢和氧2:1脱去剩余碳,C12H22O11→12C+11H2O,故A正确;B.二氧化硫具有漂白性,可以使品红溶液褪色,品红颜色变淡说明SO2有漂白性,故B正确;C.蔗糖逐渐变黑体现了浓硫酸脱水性,体积膨胀,形成疏松多孔的黑面包,碳和浓硫酸加热发生氧化还原反应,体现浓硫酸强氧化性,吸水性,故C正确;D.将气体依次通过饱和碳酸氢钠溶液、二氧化硫会反应生成二氧化碳,通入澄清石灰水,二氧化碳、二氧化硫都可以使石灰水变浑浊,气体可以是二氧化碳或二氧化硫气体,故D错误;故答案为D。

【题目】【2015宁波二模】某同学取一定量某工厂所排废水试样,进行如下实验:

已知废水试样中可能含有下表离子中若干种.
阳离子 | Ba2+、K+、NH4+、Fe2+、Fe3+、X |
阴离子 | CO32﹣、SO32﹣、NO3﹣、Y |
下列判断不正确的是( )
A.离子X是H+,离子Y是SO42﹣
B.不能确定NO3﹣是否存在与废水中
C.沉淀C是纯净物
D.废水中一定存在Fe2+、NH4+,可能存在K+