题目内容
【题目】【2017绵阳模拟】取0.1molL﹣1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2OHA+NaHCO3、2NaB+CO2+H2O2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时对应的曲线是( )
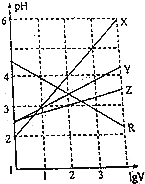
A.X是HA、Z是HB B.Y是HA、Z是HB C.Z是HA、R是HB D.Z是HA、Y是HB
【答案】B
【解析】已知:NaA+CO2+H2OHA+NaHCO3、2NaB+CO2+H2O2HB+Na2CO3,则酸性:H2CO3>HA>HCO3﹣>HB,加水稀释,促进弱酸的电离,酸性越弱,溶液稀释时pH变化越小,所以加水稀释相同的倍数时,pH变化小的是HB,由图可知,Z为HB,Y为HA,故B正确;故选B。

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案
相关题目