��Ŀ����
����Ŀ����2017÷��ģ�������������[(NH4)2Fe(SO4)26H2O]�Ƿ�����ѧ����Ҫ���Լ���ѧϰС��̽����ֽ���
(1)���鰴��ͼ1��ʾ��װ�ý���ʵ�飬�ر�ֹˮ�в�����A�е���������粒������ֽ���ȫ��������ֽ���
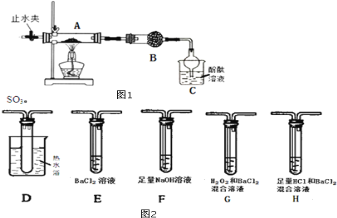
��װ��B���������� �������Լ��� ��
��װ��C�пɹ۲쵽�������� ���ɴ˿�֪��������淋ķֽ�������� ��(д��ѧʽ)
(2)����ѡ�ü���ʵ���е�װ��A��ͼ2��ʾ��װ�ý���ʵ����֤��������立ֽ�IJ����л���SO2��SO3��
������ͬѧ��ʵ��װ���У��������ӵĺ���˳��(��װ�õ���ĸ��ʾ)ΪA�� ��ȡ������������粒�����A�У�ͨ��һ��ʱ��N2�ر�ֹˮ���ٵ�ȼ�ƾ��ƣ�ͨ��N2��Ŀ���� ��
��װ��H���а�ɫ��������֤���ֽ�������� ��G�з�����Ӧ�����ӷ���ʽΪ ��
(3)���齫һ�����������������500��ʱ������������һ��ʱ������������������ʵ��֤�����˹�����ﲻ���������� ��
���𰸡�(1)�� ����� ��ʯ�� �� ��Һ����ɫ���ɫ NH3 (2)�� DHEGF���ž�װ���еĿ���(��O2)����ֹ��SO2����֤��������
�� SO3 SO2+2H2O2+Ba2+=BaSO4��+H2O+2H+ (3)ȡ�����������Թ��У���ϡ�����ܽ⣬�ٵ���KMnO4��Һ��KMnO4��Һ����ɫ
��������(1)��װ��B����״�����ÿ�֪Ϊ����ܣ�ʢ�Ź������������������[(NH4)2Fe(SO4)26H2O]�ֽ���ܵIJ���Ϊ����������������ˮ�����鰱������װ��C�еķ�̪��Һ������װ��B�dz�ȥ���ɵ����������Ϊ��ʯ����
��װ��C�пɹ۲쵽�������DZ��ɫ����������ˮ����һˮ�ϰ��������Һ�е����Լ��ԣ�������̪���ɫ��֤���ֽ�����������˰�����
(2)������ѡ�ü���ʵ���е�װ��A��ͼ2��ʾ��װ�ý���ʵ����֤��������立ֽ�IJ����л���SO2��SO3���ֽ����ͨ��װ��D��ֹ������ͨ��װ��H�е�����Ԫ�غ��Ȼ�����Һ�����Ƿ����������к���������ͨ��װ��E�������������Ƿ������ͨ��װ��G��������������������Ϊ���ᣬ��ϱ��������ɰ�ɫ���������ʣ���������������Ҫβ�����գ�������������֪װ������˳��ΪADHEGF��ȡ������������粒�����A�У�ͨ��һ��ʱ��N2�ر�ֹˮ���ٵ�ȼ�ƾ��ƣ�Ŀ���Ǹɾ�װ���е���������Զ����������ĸ�����
��װ��H���а�ɫ������˵�������˲�����ˮ����������ij���Ϊ���ᱵ������ԭ������������SO3��G�й��������������������������ᣬ������Ȼ�����Ӧ�������ᱵ��ɫ��������Ӧ�����ӷ���ʽΪ��SO2+2H2O2+Ba2+=BaSO4��+H2O+2H+��
(3)���ö��������Ӿ��л�ԭ�����ʵ����飬ʵ�����Ϊ��ȡ�����������Թ��У���ϡ�����ܽ⣬�ٵ���KMnO4��Һ��KMnO4��Һ����ɫ��