题目内容
【题目】下图示意工业集中的扩散。读图回答下列下列各题。
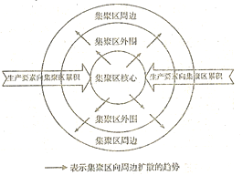
【1】下列关于集聚和分散的叙述正确的是
A.有投入和产出关系的工业应该集聚,没有投入和产出关系的工业不会集聚
B.工业集聚势必会形成工业地域
C.工业集聚可以降低成本、获得规模效益
D.工业集聚最终会形成工业分散,工业分散最终也会导致工业集聚
【2】若图中细箭头表示我国长三角地区空间扩散,则其主要原因可能是
A.政府的行政规划
B.工业企业之间联系不紧密
C.集聚核心区的饱和导致企业压力增大,成本增加
D.集聚区外围和周边地区比集聚核心区更具吸引力
【答案】
【1】D
【2】C
【解析】
试题分析:
【1】具有工业联系的一些工厂,往往发生近距离集聚,可以扩大总体生产能力,最终降低生产成本,提高利润,获得规模效益。工业的集聚与扩散是相比较而存在、相对立而发展的。一般来说,在工业化前期和中期,表现为人力、物力、财力的空间集中。到工业化后期,区域工业多表现为分散,即向工业基础较落后的地区扩散。D对。没有投入和产出关系的工业,有空间上的联系,也会集聚,A错。轻工业集聚不能形成工业地域,B错。工业集聚可以降低成本、获得规模效益,没有说出工业分散的关系,C错。
【2】图示箭头表示工业向周边地区转移。我国长三角地区工业向外转移的主要原因是产业升级以及原有区位优势的降低。所以应是集聚核心区的饱和导致企业压力增大,成本增加,C对,D错。政府的行政规划不是主要原因,A错。与工业企业之间联系无关,B错。

练习册系列答案
 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目