题目内容
【题目】【2017原州区校级二模】亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐.但因其有毒,所以在食品行业用量有严格限制.现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分.
已知:①NO+NO2+2OH﹣═2NO![]() +H2O ②气体液化的温度:NO2为21℃,NO为﹣152℃
+H2O ②气体液化的温度:NO2为21℃,NO为﹣152℃
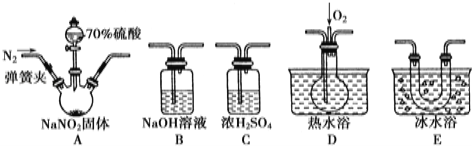
(1)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接)为A、C、 、 、 ;
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是 ;
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体.
①确认A中产生的气体含有NO,依据的现象是 ;
②装置E的作用是 ;
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为 .如果没有装置C,对实验结论造成的影响是 ;
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是 。
【答案】(1)E D B (2)防止可能生成的NO被完全氧化成NO2,造成对A中反应气体产物检验的干扰 (3)①D中出现红棕色气体 ②冷凝使NO2完全液化 (4)4NO2+O2+4NaOH=4NaNO3+2H2O;水蒸气存在,会与NO2反应产生NO,造成对NO来源于哪里的认识不清 (5)2NaNO2+H2SO4=Na2SO4+NO2↑+NO↑+H2O
【解析】(1)C吸收水蒸气,B尾气处理,防止污染空气,D检验NO,E冷却二氧化氮,利用检验NO,所以装置的连接为A→C→E→D→B;
(2)NO很容易被氧气氧化,装置中有空气,无法检验有NO生成,所以通氮气的目的是排尽整个装置中的空气,防止产生的NO被氧化生成NO2;
(3)①D中无色气体变成红色,说明含有NO气体;
②二氧化氮的液化温度是21℃,低于此温度时,二氧化氮气体变成液态;
(4)如果向D中通入过量O2,则装置B中二氧化氮、氧气和氢氧化钠反应生成硝酸钠和水,其反应方程式为:4NO2+O2+4NaOH=4NaNO3+2H2O,如果没有装置C,二氧化氮和水反应生成一氧化氮,造成干扰;
(5)通过以上分析知,该反应中生成二氧化氮、一氧化氮,同时还有硫酸钠、水生成,所以反应方程式为2NaNO2+H2SO4=Na2SO4+NO2↑+NO↑+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案