��Ŀ����
����Ŀ��[2017�¿α���]Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ���������������Ҫ�ɷ�ΪFeTiO3������������MgO��SiO2�����ʣ����Ʊ��������������£�
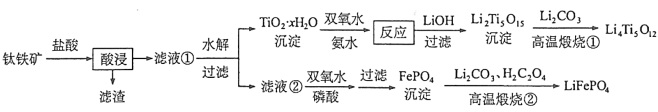
�ش��������⣺
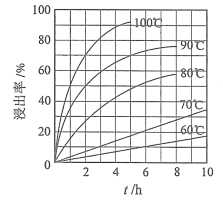
��1���������ʵ���У����Ľ����ʽ������ͼ��ʾ����ͼ��֪�������Ľ�����Ϊ70%ʱ�������õ�ʵ������Ϊ___________________��
��2���������������Ҫ��![]() ��ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ__________________��
��ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ__________________��
��3��TiO2��xH2O������˫��ˮ����ˮ��Ӧ40 min����ʵ�������±���ʾ��
�¶�/�� | 30 | 35 | 40 | 45 | 50 |
TiO2��xH2Oת����% | 92 | 95 | 97 | 93 | 88 |
����40 ��ʱTiO2��xH2Oת������ߵ�ԭ��__________________��
��4��Li2Ti5O15��Ti�Ļ��ϼ�Ϊ+4�����й���������ĿΪ__________________��
��5��������Һ������![]() ������˫��ˮ�����ᣨ����Һ�������1������ʹ
������˫��ˮ�����ᣨ����Һ�������1������ʹ![]() ǡ�ó�����ȫ����Һ��
ǡ�ó�����ȫ����Һ��![]() ����ʱ�Ƿ���Mg3(PO4)2�������ɣ� ����ʽ���㣩��FePO4��Mg3(PO4)2��Ksp�ֱ�Ϊ
����ʱ�Ƿ���Mg3(PO4)2�������ɣ� ����ʽ���㣩��FePO4��Mg3(PO4)2��Ksp�ֱ�Ϊ![]() ��
��
��6��д��������������������FePO4�Ʊ�LiFePO4�Ļ�ѧ����ʽ ��
���𰸡���1��100����2h��90����5h
��2��FeTiO3+ 4H++4Cl = Fe2++ ![]() + 2H2O
+ 2H2O
��3������40����TiO2��xH2Oת����Ӧ�������¶����߶����ӣ�����40����˫��ˮ�ֽ��백���ݳ�����TiO2��xH2Oת����Ӧ�����½�
��4��4
��5��Fe3+ǡ�ó�����ȫʱ��c(![]() )=
)=![]() mol��L1=1.3��10�C17 mol��L1��c3(Mg2+)��c2(
mol��L1=1.3��10�C17 mol��L1��c3(Mg2+)��c2(![]() )��(0.01)3��(1.3��10�C17)2=1.7��10�C40��Ksp [Mg3(PO4)2]����˲�������Mg3(PO4)2������
)��(0.01)3��(1.3��10�C17)2=1.7��10�C40��Ksp [Mg3(PO4)2]����˲�������Mg3(PO4)2������
��6��2FePO4 + Li2CO3+ H2C2O4![]() 2LiFePO4+ H2O��+ 3CO2��
2LiFePO4+ H2O��+ 3CO2��
����������1����ͼʾ��֪���������ʱ���ľ�����Ϊ70%ʱ����Ӧѡ����100����2h��90����5h�½��У�
��2���������ʱ�������ܽ�FeTiO3����![]() ʱ��������Ӧ�����ӷ���ʽΪFeTiO3+4H++4Cl��Fe2++
ʱ��������Ӧ�����ӷ���ʽΪFeTiO3+4H++4Cl��Fe2++ ![]() + 2H2O��
+ 2H2O��
��3���¶���Ӱ�����ʵ���Ҫ���أ���H2O2�ڸ������ֽ⡢��ˮ�ӷ�����ԭ���ǵ���40����TiO2��xH2Oת����Ӧ�������¶����߶����ӣ�����40����˫��ˮ�ֽ��백���ݳ�����TiO2��xH2Oת����Ӧ�����½���
��4��Li2Ti5O15��LiΪ+1�ۣ�OΪ�C2�ۣ�TiΪ+4�ۣ�������(![]() )����Ԫ���ԨC1�ۣ������������ĿΪx�������������ϼ۴�����Ϊ0����֪(+1)��2+(+4)��5+(�C2)��(15�C2x)+(�C1)��2x=0����ã�x=4��
)����Ԫ���ԨC1�ۣ������������ĿΪx�������������ϼ۴�����Ϊ0����֪(+1)��2+(+4)��5+(�C2)��(15�C2x)+(�C1)��2x=0����ã�x=4��
��5��Ksp[FePO4]=c(Fe3+)��c(![]() )=1.3��10�C2����c(
)=1.3��10�C2����c(![]() )��
)��![]() ��1.3��10�C17 mol/L��Qc[Mg3(PO4)2]��c3(Mg2+)��c2(
��1.3��10�C17 mol/L��Qc[Mg3(PO4)2]��c3(Mg2+)��c2(![]() )��(0.01)3��(1.3��10�C17)2=1.69��10�C40��1.0��10�C24����������
)��(0.01)3��(1.3��10�C17)2=1.69��10�C40��1.0��10�C24����������
��6��������FePO4��Li2CO3��H2C2O4��ϼ��ȿɵ�LiFePO4�����ݵ����غ��ԭ���غ�ɵô˷�Ӧ�Ļ�ѧ����ʽΪ2FePO4 + Li2CO3+ H2C2O4![]() 2LiFePO4+ H2O��+ 3CO2����
2LiFePO4+ H2O��+ 3CO2����

 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�