��Ŀ����
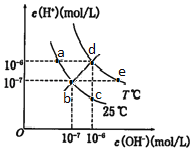
����Ŀ����2017�ҳ���У��ģ������ѧ�ϳ���AG��ʾ��Һ�е�lg![]() ��25��ʱ����0.100molL��1��NaOH��Һ�ζ�20.00mL 0.100molL��1��HNO2��Һ��AG������NaOH��Һ�����(V)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����( )
��25��ʱ����0.100molL��1��NaOH��Һ�ζ�20.00mL 0.100molL��1��HNO2��Һ��AG������NaOH��Һ�����(V)�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����( )
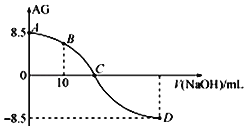
A��D����Һ��pH=11.25
B��B����Һ�д��� c(H+ )��c(OH�� )=c(NO2�� )��c(HNO2)
C��C��ʱ������NaOH��Һ�����Ϊ20 mL
D��25��ʱ��HNO2�ĵ��볣��Ka=1.0��10��55
���𰸡�A
��������A��D��lg![]() =��8.5����
=��8.5����![]() =1.0��10��8.5��KW=c(H+ )��c(OH�� )=1.0��10��14������c(H+ )=1.0��10��11.25��PH=11.25����A��ȷ��B��B����ҺΪ��Ũ�ȵ�HNO2��NaNO2��Һ����Һ�д��ڵ���غ㣺c(H+ )+c(Na+)=c(OH�� )+c(NO2�� )���������غ㣺2c(Na+)=c(HNO2)+c(NO2��)����������2�����ã�2c(H+ )��2c(OH�� )=c(NO2�� )��c(HNO2)����B����C��C��lg
=1.0��10��8.5��KW=c(H+ )��c(OH�� )=1.0��10��14������c(H+ )=1.0��10��11.25��PH=11.25����A��ȷ��B��B����ҺΪ��Ũ�ȵ�HNO2��NaNO2��Һ����Һ�д��ڵ���غ㣺c(H+ )+c(Na+)=c(OH�� )+c(NO2�� )���������غ㣺2c(Na+)=c(HNO2)+c(NO2��)����������2�����ã�2c(H+ )��2c(OH�� )=c(NO2�� )��c(HNO2)����B����C��C��lg![]() =0����
=0����![]() =1��HNO2�ĵ���̶���NaNO2��ˮ��̶���ͬ������NaOH��Һ�����С��20mL����C����D��A��lg
=1��HNO2�ĵ���̶���NaNO2��ˮ��̶���ͬ������NaOH��Һ�����С��20mL����C����D��A��lg![]() =��8.5����
=��8.5����![]() =1.0��10��8.5��KW=1.0��10��14������c2(H+)=1.0��10��5.5��HNO2�ĵ��볣��Ka=
=1.0��10��8.5��KW=1.0��10��14������c2(H+)=1.0��10��5.5��HNO2�ĵ��볣��Ka=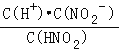 =
=![]() ����D����ѡA��
����D����ѡA��

 �¿α�ͬ��ѵ��ϵ�д�
�¿α�ͬ��ѵ��ϵ�д� һ����ʦ����Ӧ����������һ��ȫϵ�д�
һ����ʦ����Ӧ����������һ��ȫϵ�д�