题目内容
【题目】某温度下,向一定体积0.1 mol·L1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH(pOH=lg c(OH))与pH的变化关系如图所示,则
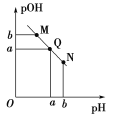
A.M点所示溶液的导电能力强于Q点
B.N点所示溶液中c(CH3COO)>c(Na+)
C.M点和N点所示溶液中水的电离程度相同
D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积
【答案】C
【解析】结合醋酸与NaOH溶液的反应,pOH、pH的定义及题给图像,分析各选项并得出合理答案。
Q点pOH=pH=a,则有c(H+)=c(OH),此时溶液呈中性,那么c(CH3COO)=c(Na+),N点溶液呈碱性,c(OH)>c(H+),那么c(CH3COO)<c(Na+),B错。结合图像可知,M点溶液中含有CH3COOH和CH3COONa,在滴加NaOH溶液的过程中,溶液中离子浓度变大,则M点溶液的导电能力比Q点弱,A错。M点pOH=b,N点pH=b,说明M点c(OH)与N点c(H+)相等,对水的电离的抑制程度相同,因此M点和N点水的电离程度相同,C对。若消耗NaOH溶液与醋酸溶液的体积相等,二者恰好反应生成CH3COONa,溶液显碱性,而Q点溶液呈中性,显然醋酸溶液的体积大于消耗NaOH溶液的体积,D错。

练习册系列答案
相关题目