题目内容
【题目】读左图、右图为两区域示意图,完成下列问题。
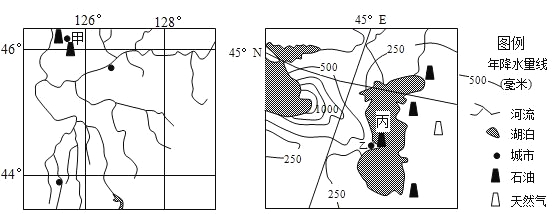
(1)简述左图所示的地区易发生洪涝灾害的自然原因 。
(2)丙湖南部盐度夏季高于冬季,试分析其主要原因 。
(3)从左图到右图同纬区域沿途主要自然景观有何变化 ?说出图示两区域的主要生态环境问题 。
(4)甲、乙两城市未来经济发展中可能面临的最大障碍是什么 ?简述两城市实现可持续发展的主要途径 。
【答案】(1)温带季风气候,夏季降水集中;地势低平,排水不畅;支流众多,干支流同时涨水;多沼泽、冻土,地下水位高。
(2)夏季气温高,湖水蒸发量大;地处内陆,降水稀少;南部径流补给少;冬季降水稍多(受西风影响)。
(3)呈现从森林-草原-荒漠的变化。
甲:过度砍伐森林(皆伐)、黑土肥力下降(水土流失)、湿地破坏等。
乙:土地荒漠化、土壤次生盐碱化、湖泊萎缩等。
(4)资源枯竭、环境污染,
延长产业链,发展高附加值石油工业;发展节水农业及特色农产品加工业;发展旅游业、高科技产业和第三产业;加强区域合作,发展国际贸易;治理污染,保护环境。
【解析】
试题分析:(1)洪涝灾害多发的原因,主要从地形、降水、排水、水系特点等条件分析。根据经纬度判断,左图所示区域位于我国东北平原,属于温带季风气候,夏季降水集中。地势低平,排水不畅。支流众多,干支流同时涨水。区域气温低,蒸发弱,多沼泽、冻土,地下水位高。
(2)根据经纬度判断,丙湖是里海。湖泊地处内陆,降水稀少,夏季气温高,湖水蒸发量大。图示湖泊支流主要在北部流入,南部径流补给少。冬季湖泊受西风影响,降水稍多。所以南部盐度夏季高于冬季。
(3)根据经度判断,从左图到右图同纬区域沿途主要自然景观变化,与从沿海到内陆的自然带变化规律一致,景观呈现从森林-草原-荒漠的变化。
甲地生态环境问题主要是过度砍伐森林,采用皆伐的方法,导致水土流失,黑土肥力下降,湿地破坏等问题。乙地生态环境问题主要是不合理耕作,导致土地荒漠化、土壤次生盐碱化、湖泊萎缩等问题。
(4)根据图例,甲乙两城市都是资源型城市,未来经济发展中可能面临的最大障碍是资源枯竭、环境污染等问题。要实现可持续发展,应参考传统工业区的改造措施。两城市要延长产业链,发展高附加值石油工业。发展节水农业及特色农产品加工业。发展旅游业、高科技产业和第三产业。加强区域合作,发展国际贸易。治理污染,保护环境等。

【题目】阅读材料,完成下列问题。
材料一:北京、成都、伦敦三地位置示意及气温曲线和降水量柱状图。
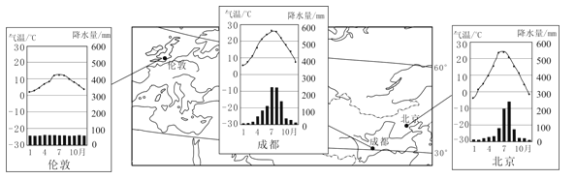
材料二:猕猴桃生长在年降水量800毫米以上的温暖湿润地区,对强光照射比较敏感,不耐旱涝。猕猴桃的生长期为210~240天,其中发芽期气温需高于10℃,结果期气温需高于20℃。
(1)英国伦敦位于亚欧大陆 侧,受盛行 风和 (填洋流性质)的影响,形成典型的温带海洋性气候。
(2)与伦敦相比,北京的气候特点是 (多项选择)。
A.全年气温变化小 | B.夏季气温高 |
C.降水量季节变化大 | D.冬季气候湿润 |
(3)与北京相比,成都冬季气温更高,其主要影响因素是 、 。
(4)北京、成都、伦敦三地中适合种植猕猴桃的是 ,并说明理由。