题目内容
【题目】实验题。
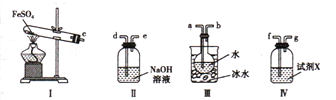
I.用下图提供的装置与试剂,组装一套CO还原CuO的实验装置,并回答问题。
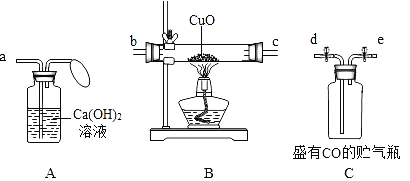
(1)使用CO气体进行实验时,可将水重新注入装置C中而将CO气体排出,此时水应从接口______(填“e”或“d”)流入,实验时气体则依次通过________→b→c→________(填接口处字母);
(2)实验开始时应该先________,后________,原因是________;
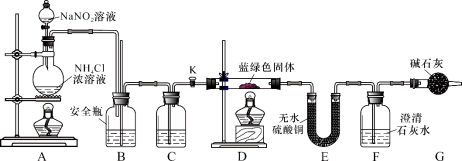
II.我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他以NaCl、NH3 、CO2等为原料先制得NaHCO3,进而生产出纯碱。有关反应的化学方程式为:NH3 + CO2 + H2O = NH4HCO3 ; NH4HCO3 + NaCl = NaHCO3↓+ NH4Cl ; 2NaHCO3 = Na2CO3 + CO2↑+ H2O
(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是__________ (填标号)。
A.碳酸氢钠难溶于水
B.碳酸氢钠受热易分解
C.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(2)某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方案实验。
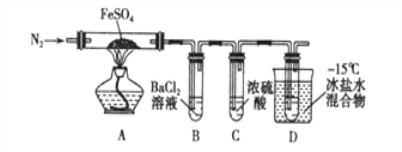
① 一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。
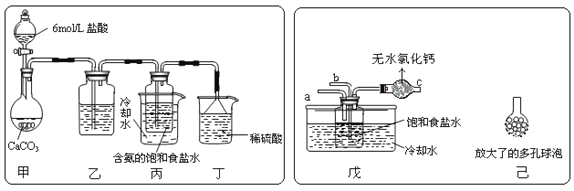
试回答下列有关问题:
(Ⅰ)乙装置中的试剂是___________;
(Ⅱ)丁装置中稀硫酸的作用是____________________。
(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是__________ (填分离操作的名称)。
② 另一位同学用图中戊装置(其它装置未画出)进行实验。
(Ⅰ)实验时,须先从____管通入_______ 气体,再从_____管中通入________气体。
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,理由是___________________________
【答案】dea通入CO加热排除玻璃管中的空气,防止CO与空气混合后加热发生爆炸C饱和碳酸氢钠溶液吸收未反应的NH3过滤aNH3bCO2增大CO2气体与溶液接触的面积,提高CO2在溶液中的吸收率
【解析】
I.(1)用水将装置C中的CO气体排除,水应从接口d流入,CO有毒,实验最后要尾气处,理实验时气体则依次通过e→b→c→a;(2)CO加热条件下与氧气反应,防止CO与空气混合后加热发生爆炸 ,要排出玻璃管中的空气,所以实验开始时应该先通入CO,后加热;II.(1)碳酸氢钠的溶解度相对氯化铵较小,碳酸氢铵与饱和食盐水反应,先析出碳酸氢钠晶体;(2)(Ⅰ)甲中排出的气体含有二氧化碳和氯化氢,为除去二氧化碳中的氯化氢,乙装置中的试剂是饱和碳酸氢钠溶液;(Ⅱ)氨气有毒,实验结束用稀硫酸吸收未反应的NH3 ;(Ⅲ)实验结束后,分离出NaHCO3 晶体的操作是过滤;②为增大二氧化碳的溶解度,需要先通入氨气,为防止倒吸,氨气从a管通入;二氧化碳从b管通入。多空球泡能增大CO2气体与溶液接触的面积,提高CO2在溶液中的吸收率。
氢气、CO等可燃性气体在还原金属氧化物时要先通入气体排出空气,再加热装置。

 全优点练单元计划系列答案
全优点练单元计划系列答案