题目内容
【题目】某元素的氯化物化学式为MCl2,现将11.1 g该氯化物溶于水配成溶液后,需用200 mL 1 mol·L-1 AgNO3溶液才能把溶液中氯离子完全沉淀。已知该M原子中有20个中子,则:
(1)计算M的质量数并写出其原子组成符号。
(2)指出M元素在周期表中的位置(周期、族)。
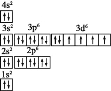
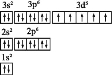
【答案】(1)40Ca
(2)第四周期ⅡA族
【解析】MCl2+2AgNO3![]() 2AgCl↓+M(NO3)2
2AgCl↓+M(NO3)2
1 2
n(MCl2) 0.2 L×1 mol·L-1
则n(MCl2)=0.1 mol
M(MCl2)=111 g·mol-1
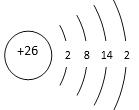
A(M)=111-35.5×2=40,Z(M)=40-20=20,M是钙元素,其原子组成符号为Ca,钙在元素周期表中位于第四周期ⅡA族。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目