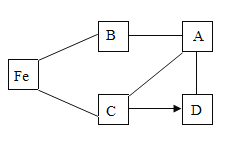
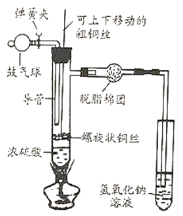
【题目】闽东毗邻东海,海洋资源十分丰富.从海水中提取氯化钠并以氯化钠和水为原料制取氢氧化钠、氯气等物质的工艺流程图如下:
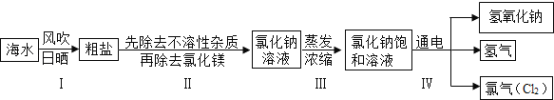
某兴趣小组进行如下实验:
(实验一)除去粗盐中的不溶性杂质
步骤一:用托盘天平称取5.0g粗盐,用药匙将该粗盐逐渐加入盛10mL水的烧杯中,边加边用玻璃棒搅拌,一直加到粗盐不再溶解为止.称量剩下的粗盐质量为1.4g
步骤二:经过过滤、蒸发,得到3.2g精盐.
(1)计算精盐的产率_________(保留一位小数).
(2)该小组测得的产率偏低,可能的原因是________.
A溶解时未充分搅拌
B蒸发时水分未蒸干
C蒸发时盐粒溅出蒸发皿
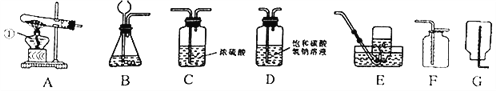
(3)步骤一、二的部分操作如图所示,其中错误的是_________(填字母序号).
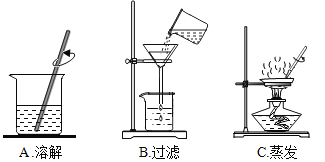
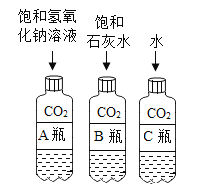
(实验二)探究工艺流程图步骤Ⅱ所得的氯化钠溶液中MgCl2是否除尽,溶液中是否含有CaCl2
[查阅资料]有关物质的溶解性表(20℃)
阴离子 | OH﹣ |
|
Ca2+ | 微 | 不 |
Mg2+ | 不 | 微 |
[进行实验]请你与他们共同完成,并回答所给的问题:
实验步骤 | 实验现象 | 实验结论 |
步骤一:取一定量的氯化钠溶液于试管中,加入适量的NaOH溶液 | 无明显现象 | 说明MgCl2______(填“已”或“未”)除尽 |
步骤二:往步骤一所得溶液中加入适量的______溶液 | 产生白色沉淀 | 说明溶液中含有CaCl2 |
[拓展思维]
(1)工艺流程图步骤Ⅰ从海水中得到粗盐,采用风吹日晒蒸发溶剂的方法,而不是采用降低溶液温度的方法,原因是________________________________.
(2)写出工艺流程图步骤Ⅳ的化学方程式__________________________.
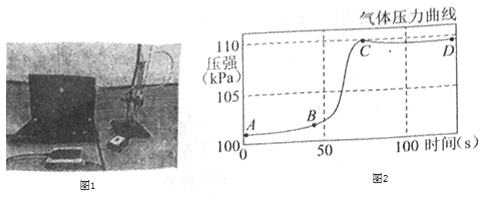
【题目】马英同学取某地石灰石样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示:
第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
生成气体的总质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
试求(反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑):
(1)m的值为 g。
(2)12g石灰石样品中碳酸钙的质量等于 g。
(3)反应完全后最终溶液中氯化钙的质量分数 。