【题目】回答下列问题:
(1)天然水中含有的部分杂质如表所示,请根据表中内容回答问题.
溶解物质 | 悬浮物质 | |
主要气体 | 主要离子 | 细菌、藻类、 |
氧气、二氧化碳、硫化氢 | 钙离子、氯离子、硫酸根离子、铝离子 | |
①表中“主要气体”中含有氧分子的有种;
②写出“主要离子”中任一种阴离子的符号;
③水中溶解的其中一种物质是氯化钙,标出氯化钙中钙元素的化合价:;
④若要除去该水样中的颜色和臭味,可加入的物质是 .
(2)现有H,N,C,O四种常见的元素,请选用其中的元素写出符合下列要求的物质各一种(用化学式表示).
①人体中含量最多的物质:;②能产生温室效应的气体:;
③点燃前需要验纯的气体:;④可充入食品包装中防腐的气体: .
【题目】空气中氧气含量测定的再认识.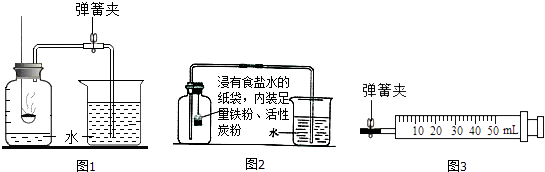
(1)【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.写出红磷燃烧的化学方程式
步骤如下:
①用弹簧夹夹紧橡皮管.
②点燃燃烧匙内的红磷,立即伸入瓶中并塞紧塞子.
③ .
④观察并记录水面的变化情况.
(2)【实验反思】多次实验,发现集气瓶内上升的水的体积始终小于瓶内原空气体积的1/5.
【实验改进1】
Ⅰ.根据铁在空气中生锈的原理(铁与氧气和水发生反应生成铁锈)设计如图2实验装置,再次测定空气中氧气含量.装置中的食盐水和活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 |
【交流表达】
① 铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁,写出该反应的化学方程式
② 根据表中数据计算,改进实验后测得的空气中氧气的体积分数是 . (消耗的水的体积忽略不计,计算结果保留一位小数).
(3)【猜想与假设】根据铁生锈的原理,某同学对最终生成的铁锈的主要成分作出猜想:
(Ⅰ)氧化铁(Ⅱ)碳酸铁,你认为猜想(填序号)一定是错误的,理由是
【实验改进2】
使用图3装置进行实验.实验前应先进行的操作
是 .
(4)【实验过程】步骤1:在注射器中放入装有足量铁粉、活性炭粉的浸有食盐水的纸袋,封闭.
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹.
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化.
【数据处理】实验中需要记录的数据是 .
计算得出氧气约占空气总体积的 ![]() .
.
(5)【计算】铁的氧化物有多种,116g四氧化三铁与多少g氧化亚铁(FeO)中所含的氧元素质量相等.(写出计算过程)
【实验评价】与燃烧红磷法相比,用改进实验测定空气中氧气含量的优点是