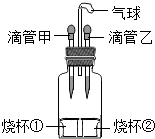
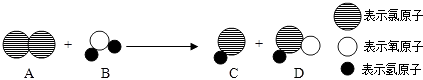
【题目】过氧化钠(Na2O2)可用作呼吸面具中的供氧剂,实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中的水和二氧化碳反应生成氧气:2Na2O2+2H2O═4NaOH+O2↑,2Na2O2+2CO2=2NaCO3+O2 .
【提出问题】过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质;假设2:过氧化钠部分变质;假设3:过氧化钠全部变质.
(1)【实验探究】
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 取部分固体于试管中,加入适量的水,在试管口插入带火星的木条 | 固体完全溶解,木条复燃 | 假设不成立 |
② | 取少量①中溶液于试管中,滴加足量的 , 振荡 | 有气泡生成 | 假设2成立 |
(2)【提出新问题】部分变质的过氧化钠样品中是否含有氢氧化钠呢?
【实验探究】
实验③:取少量①中溶液于试管中,加入足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
由实验③可以确定①中溶液含有的溶质是(填化学式).
(3)小明认为,由上述实验无法确定原固体药品中是否含有氢氧化钠,理由是 .
(4)【定量分析】
称取6.04g过氧化钠药品于锥形瓶中,加入适量蒸馏水使固体完全溶解,共收集到0.64g气体;再向上述锥形瓶中加入足量的澄清石灰水,充分反应,经过滤、干燥等操作,称量固体质量为2.00g.
写出加入澄清石灰水发生反应的化学方程式:;
(5)6.04g上述样品中含有NaOH的质量为 g.
(6)【反思提高】
过氧化钠长时间露置在空气中会全部变质,最终转化为(填化学式).
【题目】小李同学和王老师为探究人体呼出的气体和空气成分的差异,进行的实验如下:小李同学用玻璃管向盛满水的集气管中吹气,用排水法收集一瓶呼出的气体,将另一集气瓶充满新鲜的空气,将两根燃着的小木条,分别移到两只集气瓶口处,移开玻璃片,慢慢伸入集气瓶中,观察实验现象;王老师将塑料袋内的空气排尽,然后向袋内吹气,收集一定体积呼出的气体,利用仪器测定气体成分(见下表) 室内空气与正常呼吸方式呼出气体中部分气体的含量(体积分数)比较
成分 | 室内空气 | 正常呼出的气体 | 变化值 |
氧气 | 20.77% | 17.17% | 3.60% |
二氧化碳 | 0.056% | 3.67% | 3.61% |
水蒸气 | 1.98% | 2.50% | 0.52% |
(1)人呼出的气体中除含有氧气、二氧化碳、水蒸气外,还含有主要物质是;
(2)小李同学用排水法收集呼出的气体中二氧化碳的量偏小,理由是;
(3)小李同学进行实验时,发现伸入盛有如呼出气体的集气瓶中燃着的小木条先熄灭,其原因可能是(写一点即可);
(4)①由表可以看出,室内空气与正常呼出的气体相比较,(填化学式)的含量变化较大且变化值基本相同; ②人体内的氧气和许多物质发生化学反应,写出有机物(C6H10O5)和氧气反应生成二氧化碳和水的化学方程式: .