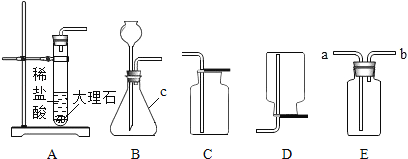
【题目】为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图.每2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,并记录前18分钟数据如下表.(碳酸钙与稀盐酸反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑)
时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
大理石碎屑生成的CO2质量/克 | 0 | 1.45 | 1.75 | 1.98 | 2.18 | 2.30 | 2.36 | 2.40 | 2.40 | 2.40 |
块状大理石生成的CO2质量/克 | 0 | 0.45 | 0.80 | 1.10 | 1.36 | 1.60 | 1.81 | 1.98 | 2.11 | 2.20 |
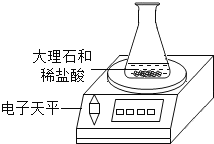
(1)实验过程中,通过观察如图装置中的哪一现象可判断反应结束? .
(2)结合表格分析,块状大理石与稀盐酸反应最多能生成多少克二氧化碳?简要说明判断的理由: .
(3)当反应进行到18分钟时,块状大理石中有多少克碳酸钙与稀盐酸发生了反应?(写出计算过程)
【题目】某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
[查阅资料]
名称 | 食用纯碱 | 食用小苏打 |
主要成分 | Na2CO3 | NaHCO3 |
酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
[实验探究]
(1)探究两者水溶液酸碱性的差异:
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变 色,但食用纯碱溶液中颜色更深,由此推测可能 溶液碱性更强.
(2)验证两种粉末的稳定性:在老师的指导下,该小组按如图所示装置进行实验操作,观察到 (填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为 ,装置中棉花的作用是 .