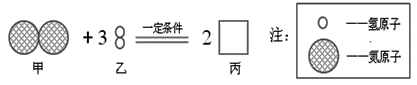
下列实验方案不能达到实验目的的是
选项 | 实验目的 | 实验方案 |
A | 鉴别氮气和二氧化碳 | 使用紫色石蕊溶液 |
B | 除去氯化钾中混有少量的氯酸钾 | 充分加热固体至质量不再减少 |
C | 验证Fe、Cu、Ag的金属活泼性 | 将铜分别伸入硫酸亚铁溶液和硝酸银溶液 |
D | 探究甲烷中仅含碳元素和氢元素 | 点燃甲烷,检验到有水和二氧化碳生成 |
A.A B.B C.C D.D
材料在交通工具上有着广泛的应用,根据下列信息回答问题。
应用 |
| 大飞机 C919 |
共享汽车 |
用到的材料 | 轮胎:橡胶 | 机翼:铝锂合金 | 车身:钢 |
(1)上述交通工具用到的材料属于金属材料的是__________ (填一种即可),属于有机合成材料的是__________。
(2)汽车车身表面的烤漆不仅美观,还能起到防锈的作用,工业上常用稀盐酸来除铁锈(Fe2O3),该反应的化学方程式是______________。
(3)化石燃料的大量使用,带来了环境的污染和资源的枯竭等问题,共享汽车在广泛推广使用乙醇汽油,其好处是___________。
某化学兴趣小组同学用铝和硝酸汞证明金属能与盐溶液反应。
(实验一)将铝箔表面打磨后,滴加硝酸汞溶液于铝箔上,发现铝表面附着银白色物质。
(1)实验前将铝箔打磨的目的是__________。
(2)发现铝表面附着银白色物质,说明汞的活泼性比铝_________(填“强”或“弱”)
(实验二)用滤纸将表面的剩余硝酸汞溶液吸去,发现铝箔上很快长出长长的“白毛”。
(3)铝箔表面的“白毛”是什么,引起了同学们的兴趣,大家决定通过实验探究它的成分。
(提出问题)铝箔表面的“白毛”是什么?
(假设与猜想)①可能是金属铝; ②可能是金属汞; ③可能是氧化铝
(查阅资料)①常温下铝在空气中发生缓慢氧化,温度升高,接触面积增大,氧气浓度增加会加快反应速率;②铝能“溶解”在汞中。
(实验及结论)
实验步骤 | 实验现象 | 实验结论 |
将“白毛”刮下装入试管中,滴加足量的稀盐酸 | Ⅰ._________________ Ⅱ._______________________ | 排除猜想①②,猜想③ 是正确的 |
(实验解释)铝箔表面很快产生“白毛”的原因_______________。
某化学小组用熟石灰配制石灰水时,发现装满熟石灰的塑料试剂瓶已经破埙.
提出向题1 试剂是否变质?
猜想 ①没有变质,成分是氢氧化钙 ②全部变质,成分是碳酸钙
③部分变质,成分是氢氧化钙和碳酸钙
进行实验1
步骤 | 操 作 | 现 象 | 结论 |
1 | 取样品于试管中,加水,滴入2~3滴酚酞试液 | ____________________________________________ | 猜想③正确 |
2 | 向试管中继续 加入过量的___________ | ____________________________________________ |
提出问题2 如何测定试剂中碳酸钙的质量分数?
进行实验2 小丽同学设计了如图所示装置进行碳酸钙的质量分数测定:

取一定质量的样品放入锥形瓶中,加入过量稀盐酸(不考虑稀盐酸的挥发),测量装置C在反应前后的总质量,即可计算出试剂中碳酸钙的质量分数。请写出稀盐酸与碳酸钙发生反应的化学方程式 ____________________________________________
说明:装置气密性良好,操作无误,各步反应完全。
反思与评价
(1)小文同学认为小丽得到的结果有较大的误差,理由是_________________________________
(2)小文同学用图E、F所示装置(注射器活塞的摩擦力很小,忽略不计)完成测量。注
射器除了贮存、加注稀盐酸外,还有的作用是____________________________________________
交流与讨论 实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成。
(1)同学们将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是______________________
(2)经实验确认废液成分,处理后绿色排放