题目内容
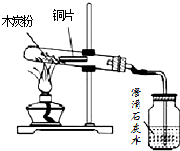 某小组在探究木炭的还原性时,发现实际操作中,采用氧化铜粉末对实验效果有很大影响,小明同学对木炭还原氧化铜的实验进行了改进,其操作步骤如下:
某小组在探究木炭的还原性时,发现实际操作中,采用氧化铜粉末对实验效果有很大影响,小明同学对木炭还原氧化铜的实验进行了改进,其操作步骤如下:①取一片长约7~8cm,宽约1cm的铜片,把表面可能存在的氧化物用砂纸除去使其表面呈光亮的紫红色;
②用洒精灯将上述铜片烧到红热后,立即伸入到集满氧气的集气瓶中,观察到的现象为:铜片表面变成
黑
黑
色;③在一支干燥的大试管中装入一定量的经烘干处理过的木炭粉,再将经过②处理过的铜片部分埋入木炭粉中;
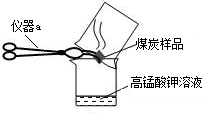
④按照右图所示的装置图连接好各种仪器;
⑤加热大试管,其中发生的反应的化学热方程式为:
C+2CuO
2Cu+CO2↑
| ||
C+2CuO
2Cu+CO2↑
,当观察到澄清石灰水
| ||
变浑浊
变浑浊
后,先移走导管,后停止加热;⑥待试管冷却后,用镊子取出铜片,洗净后观察.根据上述实验步骤,回答下列问题:
(1)填写上述各空.
(2)⑤中“先”、“后”颠倒,造成的后果是:
石灰水倒吸入大试管中,使试管炸裂
石灰水倒吸入大试管中,使试管炸裂
.(3)⑥中观察到的现象是:铜片表面埋入木炭粉的部分
由黑色变成光亮的紫红色
由黑色变成光亮的紫红色
.分析:(1)②铜和氧气在加热的条件下可反应生成氧化铜,铜是红色的,氧化铜是黑色的;
⑤碳和氧化铜反应生成铜和二氧化碳,据此书写方程式,二氧化碳可使澄清石灰水变浑浊;
(2)若先停止加热,则试管内温度降低,气压减小,石灰水会倒流入试管内,引起试管炸裂;
(3)木炭具有还原性,可将氧化铜还原为红色的铜.
⑤碳和氧化铜反应生成铜和二氧化碳,据此书写方程式,二氧化碳可使澄清石灰水变浑浊;
(2)若先停止加热,则试管内温度降低,气压减小,石灰水会倒流入试管内,引起试管炸裂;
(3)木炭具有还原性,可将氧化铜还原为红色的铜.
解答:解:(1)②铜和氧气在加热的条件下可反应生成氧化铜,铜是红色的,氧化铜是黑色的,所以将铜片烧到红热后,立即伸入到集满氧气的集气瓶中,可观察到铜片表面变成黑色;
⑤木炭具有还原性,和氧化铜加热反应生成铜和二氧化碳,反应方程式是C+2CuO
2Cu+CO2↑,生成的二氧化碳可使澄清石灰水变浑浊;
(2)若先停止加热,则试管内温度降低,气压减小,石灰水会倒流入试管内,引起试管炸裂;
(3)木炭具有还原性,可将氧化铜还原为红色的铜,所以铜片表面埋入木炭粉的部分将变红,未埋入的部分则依然是黑色;
故答案为:
(1)黑; C+2CuO
2Cu+CO2↑;变浑浊;
(2)石灰水倒吸入大试管中,使试管炸裂;
(3)由黑色变成光亮的紫红色.
⑤木炭具有还原性,和氧化铜加热反应生成铜和二氧化碳,反应方程式是C+2CuO
| ||
(2)若先停止加热,则试管内温度降低,气压减小,石灰水会倒流入试管内,引起试管炸裂;
(3)木炭具有还原性,可将氧化铜还原为红色的铜,所以铜片表面埋入木炭粉的部分将变红,未埋入的部分则依然是黑色;
故答案为:
(1)黑; C+2CuO
| ||
(2)石灰水倒吸入大试管中,使试管炸裂;
(3)由黑色变成光亮的紫红色.
点评:铜在加热的条件下生成黑色的氧化铜,木炭具有还原性,氧化铜与木炭可反应生成铜,同时结合实验注意事项分析解答.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
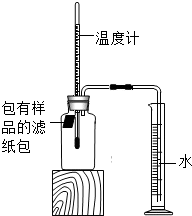 某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:
某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:如图所示(该装置气密性良好),室温时,将包有样品的滤纸包用大头针固定在橡皮塞上,迅速塞紧橡皮塞.已知,此集气瓶净容积为146mL.一段时间后,观察到量筒内水沿导管进入集气瓶.当温度恢复至室温,且量筒内水面高度不再发生变化时读数(此时瓶内氧气含量近似为零).
记录起始和最终量筒的读数以及所需时间如下表.
| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| Ⅰ | 1g铁粉、0.2g木炭粉和10滴水 | 100 | 70 | 约120 |
| Ⅱ | l g铁粉、0.2g木炭粉、10滴水和少量氯化钠 | 100 | 70 | 约70 |
实验过程中,温度计示数如何变化.
实验结束后取出Ⅰ号样品滤纸包,打开.可观察到样品的颜色变为
(2)分析实验Ⅰ和Ⅱ所得数据,初步推断铁锈蚀的速率与
(3)该实验还可测量空气中氧气的含量.根据实验数据计算氧气约占空气体积的
(4)现要增加一个对比实验,探究木炭对铁锈蚀速率的影响,则需增加实验的样品组成为
燃烧是一种发光、发热的剧烈的化学反应.认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的.
(1)物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,另外两个条件分别是 ; .
(2)下面是验证燃烧条件的实验装置图.
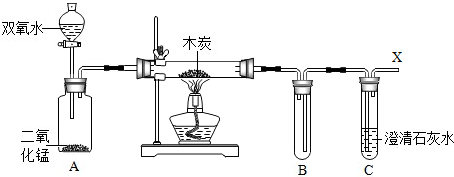
已知木炭是一种可燃物.请验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧(两个条件须分别验证),只有同时具备这两个条件才能发生燃烧.
某化学实验小组已经在完成气密性的检查后为你填装好了药品,并在整个装置中充满了氮气.请你继续设计实验步骤完成后续探究,要求实验过程中不得拆、装仪器.
(3)①装置A中发生反应的化学方程式为 .
②装置B在“盖灭酒精灯,待仪器恢复到常温”这一步中的作用是 .
③小华同学认为,x处的气体不应直接排放到空气中去,大家经讨论后认为很有道理,你认为其中的道理是: .
(1)物质燃烧一般需要同时满足三个条件,物质具有可燃性是燃烧的首要条件,另外两个条件分别是
(2)下面是验证燃烧条件的实验装置图.

已知木炭是一种可燃物.请验证:木炭发生燃烧的另外两个条件中,缺少任何一个条件都不能燃烧(两个条件须分别验证),只有同时具备这两个条件才能发生燃烧.
某化学实验小组已经在完成气密性的检查后为你填装好了药品,并在整个装置中充满了氮气.请你继续设计实验步骤完成后续探究,要求实验过程中不得拆、装仪器.
| 步骤 | 操作 | 预计现象及得出的结论 |
| ① | 澄清石灰水未变浑,说明燃烧还需要氧气 | |
| ② | 盖灭酒精灯.待仪器恢复到常温 | / |
| ③ | ||
| ④ | 点燃酒精灯加热,继续通氧气 |
②装置B在“盖灭酒精灯,待仪器恢复到常温”这一步中的作用是
③小华同学认为,x处的气体不应直接排放到空气中去,大家经讨论后认为很有道理,你认为其中的道理是:
(2011?武汉模拟)某校化学兴趣小组在探究铁的锈蚀条件后发现该实验耗时较长.为解决此问题,在教师的指导下进行了更深入的探究.探究过程如下:
如图所示(该装置气密性良好),室温时,将包有样品的滤纸包用大头针固定在橡皮塞上,迅速塞紧橡皮塞.已知,此集气瓶净容积为146mL.一段时间后,观察到量筒内水沿导管进入集气瓶.当温度恢复至室温,且量筒内水面高度不再发生变化时读数(此时瓶内氧气含量近似为零).
记录起始和最终量筒的读数以及所需时间如下表.
(1)根据所学知识推测:
实验过程中,温度计示数如何变化.______;
实验结束后取出Ⅰ号样品滤纸包,打开.可观察到样品的颜色变为______.
(2)分析实验Ⅰ和Ⅱ所得数据,初步推断铁锈蚀的速率与______ 有关(填化学式).
(3)该实验还可测量空气中氧气的含量.根据实验数据计算氧气约占空气体积的______%(计算结果精确到0.1%).
(4)现要增加一个对比实验,探究木炭对铁锈蚀速率的影响,则需增加实验的样品组成为______.

如图所示(该装置气密性良好),室温时,将包有样品的滤纸包用大头针固定在橡皮塞上,迅速塞紧橡皮塞.已知,此集气瓶净容积为146mL.一段时间后,观察到量筒内水沿导管进入集气瓶.当温度恢复至室温,且量筒内水面高度不再发生变化时读数(此时瓶内氧气含量近似为零).
记录起始和最终量筒的读数以及所需时间如下表.
| 序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
| Ⅰ | 1g铁粉、0.2g木炭粉和10滴水 | 100 | 70 | 约120 |
| Ⅱ | l g铁粉、0.2g木炭粉、10滴水和少量氯化钠 | 100 | 70 | 约70 |
实验过程中,温度计示数如何变化.______;
实验结束后取出Ⅰ号样品滤纸包,打开.可观察到样品的颜色变为______.
(2)分析实验Ⅰ和Ⅱ所得数据,初步推断铁锈蚀的速率与______ 有关(填化学式).
(3)该实验还可测量空气中氧气的含量.根据实验数据计算氧气约占空气体积的______%(计算结果精确到0.1%).
(4)现要增加一个对比实验,探究木炭对铁锈蚀速率的影响,则需增加实验的样品组成为______.


 ”.然而化学方程式中最后一种物质的化学式印刷不清楚,根据上下文了解到该物质是一种酸,请根据已学知识推测其化学式:
”.然而化学方程式中最后一种物质的化学式印刷不清楚,根据上下文了解到该物质是一种酸,请根据已学知识推测其化学式: