题目内容
实验室制取氧气的实践与研究.
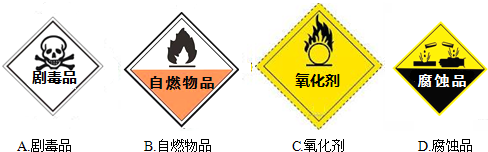
(1)过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性.贮运过氧化氢的试剂箱上最适合粘贴的一张标识是

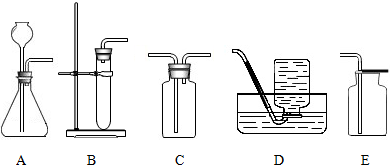
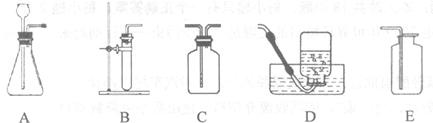
(2)过氧化氢溶液常用于实验室制取氧气.可供选择的仪器或装置如图2所示.
①要以过氧化氢为原料制取氧气,应选择气体发生装置为
②MnO2可以连续反应使用,因为MnO2在反应前后
③用D收集氧气,验证收集的氧气是否满的方法是
(3)生产火箭燃料的工业废水中含有少量偏二甲肼X,可用双氧水处理排污,反应的化学方程式为X+8H2O2=2CO2↑+N2↑+12H2O,则X的化学式为
(1)过氧化氢是一种无色透明的无毒液体,过氧化氢溶液俗称“双氧水”,具有强氧化性.贮运过氧化氢的试剂箱上最适合粘贴的一张标识是
C
C
(从图1中选填字母序号).
(2)过氧化氢溶液常用于实验室制取氧气.可供选择的仪器或装置如图2所示.
①要以过氧化氢为原料制取氧气,应选择气体发生装置为
B
B
(选填字母A~E);反应的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
②MnO2可以连续反应使用,因为MnO2在反应前后
质量
质量
和化学性质
化学性质
都不变;③用D收集氧气,验证收集的氧气是否满的方法是
将带火星的木条放于集气瓶口,若木条复燃则收集满了
将带火星的木条放于集气瓶口,若木条复燃则收集满了
.(3)生产火箭燃料的工业废水中含有少量偏二甲肼X,可用双氧水处理排污,反应的化学方程式为X+8H2O2=2CO2↑+N2↑+12H2O,则X的化学式为
C2N2H8
C2N2H8
.分析:(1)从过氧化氢的化学性质进行分析;
(2)①根据反应物的状态和反应条件确定发生装置,并据反应原理书写方程式;
②根据二氧化锰是过氧化氢分解的催化剂,及催化剂的概念分析解答;
③根据氧气验满的方法进行解答;
(3)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,进行解答.
(2)①根据反应物的状态和反应条件确定发生装置,并据反应原理书写方程式;
②根据二氧化锰是过氧化氢分解的催化剂,及催化剂的概念分析解答;
③根据氧气验满的方法进行解答;
(3)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,进行解答.
解答:解:(1)从过氧化氢的化学性质分析:过氧化氢具有强氧化性.所以贮运过氧化氢的试剂箱上最适合粘贴的一张标识是 C;
(2)①过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应的反应物的状态是固态和液态,反应条件是常温,故选固液常温型的发生装置,反应方程式是:2H 2O 2
2H2O+O 2↑;
②二氧化锰是过氧化氢制氧气的催化剂,催化剂在化学反应前后质量和化学性质都不变;
③根据氧气验满的方法:带火星的木条放于瓶口,木条复燃,即收集满了;
(3)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,依据反应的化学方程式为
X+8H2O2=2CO2↑+N2↑+12H2O,推测X的化学式为:C2N2H8;
故答案为:(1)C;
(2)①B;2H 2O 2
2H2O+O 2↑;
②质量;化学性质;
③将带火星的木条放于集气瓶口,若木条复燃则收集满了;
(3)C2N2H8 .
(2)①过氧化氢在二氧化锰的催化作用下分解生成水和氧气,该反应的反应物的状态是固态和液态,反应条件是常温,故选固液常温型的发生装置,反应方程式是:2H 2O 2
| ||
②二氧化锰是过氧化氢制氧气的催化剂,催化剂在化学反应前后质量和化学性质都不变;
③根据氧气验满的方法:带火星的木条放于瓶口,木条复燃,即收集满了;
(3)根据质量守恒定律:在化学反应中,反应前后原子的种类没有改变,数目没有增减,依据反应的化学方程式为
X+8H2O2=2CO2↑+N2↑+12H2O,推测X的化学式为:C2N2H8;
故答案为:(1)C;
(2)①B;2H 2O 2
| ||
②质量;化学性质;
③将带火星的木条放于集气瓶口,若木条复燃则收集满了;
(3)C2N2H8 .
点评:该题从实验室制取氧气的实践出发,考查了过氧化氢的性质,制取氧气的原理,发生装置的选取,验满等知识,并考查了质量守恒定律的应用,对于学生掌握制取氧气的方法以及实践活动有积极的指导意义.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目