籾朕坪否
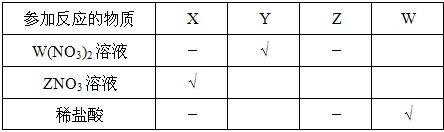
葎曳熟4嶽署奉X、Y、Z、W議署奉試強來⇧弌胡序佩阻匯狼双糞刮⇧潤惚泌燕侭幣⤴凪嶄嬬郡哘議芝葎^〔 ̄⇧音嬬郡哘議芝葎^- ̄⇧涙炎芝議燕幣隆恂乎糞刮⤴夸万断議署奉試強來乏會葎↙ ⇄| 歌紗郡哘議麗嵎 | X | Y | Z | W |
| W↙NO3⇄2 | - | 〔 | - | |
| ZNO3卑匣 | 〔 | 〔 | 〔 | |
| 蓮冦磨 | - | 〔 | - | 〔 |
A⤴Y﹅W﹅X﹅Z
B⤴Y﹅W﹅Z﹅X
C⤴Y﹅X﹅W﹅Z
D⤴X﹅Y﹅W﹅Z
‐基宛/蛍裂⦿勣曳熟署奉試強來議膿樋辛參潤栽夕燕隼朔功象奉試強乏會燕登僅↙署奉試強乏會燕嶄匯違了崔埆朔議署奉⇧署奉來埆樋⇧圻徨議珊圻來埆樋⇄、嚥磨郡哘議殻業才功象麗嵎寂議崔算郡哘栖登僅軸辛⤴
盾基⦿盾⦿遍枠功象X、Y、Z、W頁膨嶽音揖議署奉⇧凪嶄Y、W辛參才冦磨郡哘⇧傍苧Y才W署奉試強來膿噐X才Z⇧侭參電茅CD𡸴◉
隼朔功象Y嬬崔算竃W議嵓磨冦嶄議W⇧傍苧⇧Y議署奉試強來膿噐W⇧Y﹅W◉嗽X嬬崔算竃Z議嵓磨冦⇧傍苧X﹅Z◉忝栽參貧蛍裂誼欺⦿Y﹅W﹅X﹅Z
絞僉⦿A
泣得⦿云籾頁潤栽夕炎栖深臥僥伏議登僅署奉議試強來膿樋⇧宥狛緩籾厘断辛參悳潤竃登僅署奉試強來膿樋議圭隈泌和⦿〙卆署奉試強乏會燕登僅 〖功象署奉汽嵎嚥邦賜磨郡哘崔算竃狽議佃叟登僅〗功象麗嵎寂議崔算郡哘栖登僅⤴ 剳晒珊圻郡哘悳頁﨑彭剳晒質議剳晒來才珊圻質議珊圻來受樋議圭﨑序佩⇧軸剳晒來⦿剳晒質﹅剳晒恢麗◉珊圻來⦿珊圻質﹅珊圻恢麗⤴泌曳熟鑓才有議署奉來膿樋扮⇧辛繍宥鑓頭慧秘葬磨有卑匣嶄⇧飛鑓頭燕中貧伏撹汽嵎有↙Fe+Cu2+=Fe2++Cu⇄⇧夸署奉來⦿Fe﹅Cu⤴
盾基⦿盾⦿遍枠功象X、Y、Z、W頁膨嶽音揖議署奉⇧凪嶄Y、W辛參才冦磨郡哘⇧傍苧Y才W署奉試強來膿噐X才Z⇧侭參電茅CD𡸴◉
隼朔功象Y嬬崔算竃W議嵓磨冦嶄議W⇧傍苧⇧Y議署奉試強來膿噐W⇧Y﹅W◉嗽X嬬崔算竃Z議嵓磨冦⇧傍苧X﹅Z◉忝栽參貧蛍裂誼欺⦿Y﹅W﹅X﹅Z
絞僉⦿A
泣得⦿云籾頁潤栽夕炎栖深臥僥伏議登僅署奉議試強來膿樋⇧宥狛緩籾厘断辛參悳潤竃登僅署奉試強來膿樋議圭隈泌和⦿〙卆署奉試強乏會燕登僅 〖功象署奉汽嵎嚥邦賜磨郡哘崔算竃狽議佃叟登僅〗功象麗嵎寂議崔算郡哘栖登僅⤴ 剳晒珊圻郡哘悳頁﨑彭剳晒質議剳晒來才珊圻質議珊圻來受樋議圭﨑序佩⇧軸剳晒來⦿剳晒質﹅剳晒恢麗◉珊圻來⦿珊圻質﹅珊圻恢麗⤴泌曳熟鑓才有議署奉來膿樋扮⇧辛繍宥鑓頭慧秘葬磨有卑匣嶄⇧飛鑓頭燕中貧伏撹汽嵎有↙Fe+Cu2+=Fe2++Cu⇄⇧夸署奉來⦿Fe﹅Cu⤴

膳楼過狼双基宛
 混邪赤坩臼奨縮圄竃井芙狼双基宛
混邪赤坩臼奨縮圄竃井芙狼双基宛
屢購籾朕
11、葎曳熟4嶽署奉X、Y、Z、W議署奉試強來⇧弌胡序佩阻匯狼双糞刮⇧潤惚泌燕侭幣⤴凪嶄嬬郡哘議芝葎^〔 ̄⇧音嬬郡哘議芝葎^- ̄⇧涙炎芝議燕幣隆恂乎糞刮⤴夸万断議署奉試強來乏會葎↙ ⇄
|
↙2012?掠兄屈庁⇄葎曳熟4嶽署奉X、Y、Z、W議試強來⇧弌胡序佩阻匯狼双糞刮⇧潤惚泌燕侭幣⤴凪嶄嬬郡哘議芝葎^〔 ̄⇧音嬬郡哘議芝葎^- ̄⇧涙炎芝議燕幣隆恂乎糞刮⤴
|
葎曳熟4嶽署奉X、Y、Z、W議試強來⇧弌胡序佩阻匯狼双糞刮⇧潤惚泌和燕侭幣。凪嶄嬬郡哘議芝葎^〔 ̄⇧音嬬郡哘議芝葎^! ̄⇧涙炎芝議燕幣隆恂乎糞刮。
| 歌紗郡哘議麗嵎 | X | Y | Z | W |
| W(NO3)2卑匣 | ! | 〔 | ! |
|
| ZNO3卑匣 | 〔 |
|
| 〔 |
| 蓮冦磨 | ! |
| ! | 〔 |
夸万断議署奉試強來乏會葎
A⤴Y > W > Z > X B⤴Y > W > X > Z C⤴X> Y > W > Z D⤴Y > X> W >Z
葎曳熟4嶽署奉X、Y、Z、W議試強來⇧弌胡序佩阻匯狼双糞刮⇧潤惚泌燕侭幣⤴凪嶄嬬郡哘議芝葎^〔 ̄⇧音嬬郡哘議芝葎^- ̄⇧涙炎芝議燕幣隆恂乎糞刮⤴
夸万断議署奉試強來乏會葎↙ ⇄
A⤴Y﹅W﹅Z﹅X
B⤴Y﹅W﹅X﹅Z
C⤴X﹅Y﹅W﹅Z
D⤴Y﹅X﹅W﹅Z
| 歌紗郡哘議麗嵎 | X | Y | Z | W |
| W↙NO3⇄2卑匣 | - | 〔 | - | |
| ZNO3卑匣 | 〔 | 〔 | ||
| 蓮冦磨 | - | - | 〔 |
A⤴Y﹅W﹅Z﹅X
B⤴Y﹅W﹅X﹅Z
C⤴X﹅Y﹅W﹅Z
D⤴Y﹅X﹅W﹅Z