题目内容
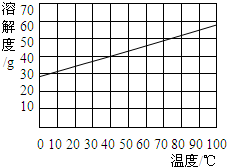 KCl的溶解度曲线如图所示:
KCl的溶解度曲线如图所示:(1)在40C时,100g水中最多可以溶解KCl
(2)在20℃时,60g水中溶解KCl a g后就不能再溶解了,则溶解KCl a g后形成的溶液属于
(3)上述20℃、60g水中不能再溶液KCl时,形成的溶液其溶质质量分数为(用含%的计算式表示)
分析:根据物质的溶解度曲线,某温度时某物质的溶解度大小;可以判断溶液是否饱和;溶液中溶质的质量分数=
×100%,溶液稀释前后,溶质的质量不变.
| 溶质质量 |
| 溶液质量 |
解答:解:(1)40C时,KCl的溶解度为40g,故40C时,100g水中最多可以溶解KCl 40g;
(2)在20℃时,60g水中溶解KCl a g后就不能再溶解了,说明该温度下溶液达到了饱和状态.
(3)20℃、60g水中不能再溶液KCl时,说明该温度下溶液达到了饱和状态.溶质的质量分数为:
%,使其溶质的质量分数变为原来的一半,可设需加水的质量为y,则
(60+a+x)×
%=(60+a)×
%,
y=(60+a)g
故答案为:80g
故答案为:(1)40
(2)饱和
(3)
%(或
或
×100%);60+a
(2)在20℃时,60g水中溶解KCl a g后就不能再溶解了,说明该温度下溶液达到了饱和状态.
(3)20℃、60g水中不能再溶液KCl时,说明该温度下溶液达到了饱和状态.溶质的质量分数为:
| 100a |
| 60+a |
(60+a+x)×
| 50a |
| 60+a |
| 100a |
| 60+a |
y=(60+a)g
故答案为:80g
故答案为:(1)40
(2)饱和
(3)
| 100a |
| 60+a |
| a |
| 60+a |
| a |
| 60+a |
点评:主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:
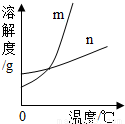
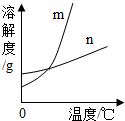
(1)依据上表数据,已经绘出KNO3和KCl的溶解度曲线如图,图中能表示KNO3溶解度曲线的是 .(填“m”或“n”)
(2)10℃时,将50g溶质质量分数为10%的KCl溶液配制为质量分数为5%的溶液,加水质量为 g.
(3)根据溶解度曲线可以知道,若从m的饱和溶液中析出晶体,应该采用 结晶的方法.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.6 | 37 | 40.0 | 42.6 | 45.5 | 48.3 | |
(2)10℃时,将50g溶质质量分数为10%的KCl溶液配制为质量分数为5%的溶液,加水质量为 g.
(3)根据溶解度曲线可以知道,若从m的饱和溶液中析出晶体,应该采用 结晶的方法.

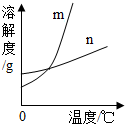 (2013?许昌一模)KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:
(2013?许昌一模)KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:
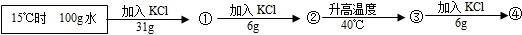
 (2013?息县三模)KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
(2013?息县三模)KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题: