题目内容
【题目】某化学兴趣小组在老师指导下制取、干燥、收集氨气,并探究氨气的一些性质。
资料卡片:氨气通常情况下是有刺激性气味的无色气体,密度比空气小,极易溶于水,易液化,液氨可作制冷剂。 加热熟石灰和氯化铵固体混合物的方法可以发生复分解反应生成氨气。如要快速产生氨气,可以将浓氨水滴加到生石灰中得到。
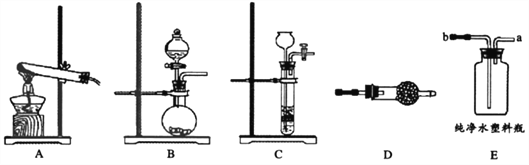
(1)利用A装置制取氨气的化学方程式为_______________。将浓氨水滴加到生石灰中快速产生氨气,发生装置最好选用________(选填装置编号)。
(2)干燥氨气可以将气体通过装有_____(填化学式)的装置D。
(3)兴趣小组计划用E装置收氨气,简述判断氨气已经集满的方法____________。
(4)按下图连接仪器后,计划在纯净水塑料瓶内引发“喷泉”,你会采取的操作是__________。
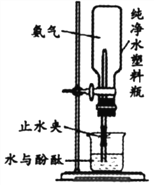
(5)试验后为处理纯净水塑料瓶内存在的氨水(NH3·H2O)可以加入少量稀硫酸,发生反应的化学方程式为_________________。
【答案】 (1)Ca(OH)2+2NH4Cl=CaCl2+2H2O+2NH3↑ (2)B (3)CaO或NaOH (4)将湿润的红色石蕊试纸放在b端,若试纸变蓝色,说明氨气已经集满 (5)打开止水夹,挤压塑料瓶,使氨气排入水中 (6)2NH3H2O+H2SO4=(NH4)2SO4+2H2O
【解析】(1)利用A装置制取氨气的化学方程式为:Ca(OH)2+2NH4Cl=CaCl2+2H2O+2NH3↑;将浓氨水滴加到生石灰快速产生氨气,发生装置最好选用B装置;(2)干燥氨气可以将气体通过装有CaO或NaOH的装置D;(3)判断氨气已经集满的方法是:将湿润的红色石蕊试纸放在b端,若试纸变蓝色,说明氨气已经集满;(4)采取的操作是:打开止水夹,挤压塑料瓶,使氨气排入水中,瓶内压强减小,烧杯中的液体会被吸入塑料瓶内;(5)氨水和浓硫酸反应的化学方程式为:2NH3H2O+H2SO4=(NH4)2SO4+2H2O。

 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
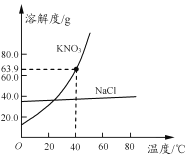
计算高手系列答案【题目】已知硝酸钾在不同温度下的溶解度如下表:
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度/g | 32 | 46 | 64 | 85.5 | 110 | 138 | 170 |
甲是80℃含有100 g水的KNO3溶液,操作过程如下图所示。以下分析错误的是
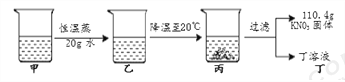
A. 甲、乙、丙、丁四种溶液中,饱和溶液只有2种
B. 甲到乙的过程中,溶质质量没有改变
C. 甲溶液中,溶剂与溶质的质量比为25: 34
D. 甲溶液冷却时,开始析出固体的温度在60℃~70℃之间