题目内容
【题目】知识整合是巩固化学知识的一种重要手段,请看下面某同学的知识整合。
已知A是一种白色固体,B和M 均是黑色固体,E和F均为常见的无色液体,C是实验室常见的气体,H为淡黄色的固体粉末。请完成下列问题:
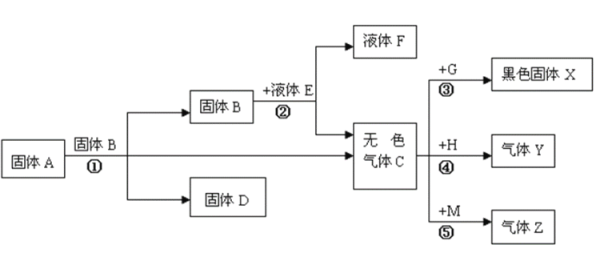
(1)写出下列物质的名称:A是____________, E是____________,X是____________
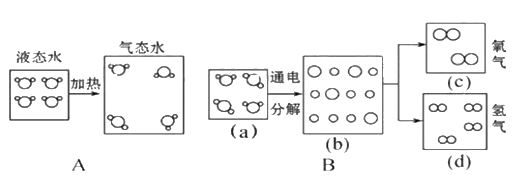
(2)反应①的符号表达式为___________________________,
反应①、②的共同点有(答一点)____________________________________。
(3)反应③的符号表达式为___________________________,基本反应类型是____________。
(4)反应③的主要实验现象是_____________________________________。
请写出反应③的注意事项________________________________________(写一点)
(5)物质都有两面性,请分别说出气体C有利的一面是________________________,气体C不利的一面是___________________________。
【答案】氯酸钾过氧化氢四氧化三铁KClO3![]() KCl+O2都是分解反应或都生成氧气Fe+O2
KCl+O2都是分解反应或都生成氧气Fe+O2![]() Fe3O4化合反应剧烈燃烧,火星四射,放出大量的热,生成黑色固体在集气瓶底铺少量水或薄层沙或铁丝绕成螺旋状等供给呼吸等使金属锈蚀等
Fe3O4化合反应剧烈燃烧,火星四射,放出大量的热,生成黑色固体在集气瓶底铺少量水或薄层沙或铁丝绕成螺旋状等供给呼吸等使金属锈蚀等
【解析】
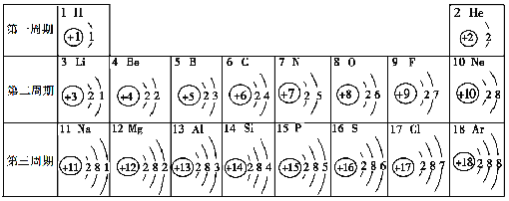
首先:找到解题突破口-解题关键,然后:“顺藤摸瓜”进行顺推、逆推或顺、逆推相结合,得出结论;最后:代入原题检验;找到解题突破口:H为淡黄色的固体粉末,为硫;根据A是一种白色固体,B和M均是黑色固体,E和F均为常见的无色液体,C是实验室常见的气体,则推测A是氯酸钾,B为二氧化锰,M是碳,E为过氧化氢,F为水,C为氧气,D为氯化钾,G为铁,X为四氧化三铁,Y为二氧化硫,代入原题检验。
(1)根据分析,可知:A是氯酸钾,E是过氧化氢,X是四氧化三铁;
(2)反应①为氯酸钾分解生成氯化钾和氧气,反应的符号表达式为:KClO3![]() KCl+O2;反应②为过氧化氢分解生成水和氧气,故其共同点有为分解反应或生成氧气;
KCl+O2;反应②为过氧化氢分解生成水和氧气,故其共同点有为分解反应或生成氧气;
(3)反应③铁丝在氧气中燃烧生成四氧化三铁,反应的符号表达式为Fe+O2![]() Fe3O4,基本反应类型是化合反应;
Fe3O4,基本反应类型是化合反应;
(4)反应③铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成黑色固体;做铁丝燃烧应注意的问题是:为防止生成物熔化溅落下来,使瓶底炸裂,在集气瓶底铺少量水或薄层沙或铁丝绕成螺旋状等;
(5)物质都有两面性,气体C氧气有利的一面是供给呼吸,支持燃烧,气体C不利的一面是使金属氧化、锈蚀。

 阅读快车系列答案
阅读快车系列答案【题目】被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的过氧化氢(H2O2),通常情况下均为无色液体。在化学实验中都有很重要的作用。
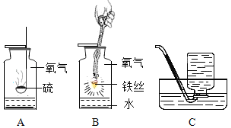
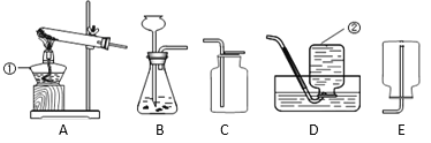
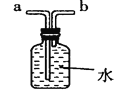
(1)指出下列实验容器中水的主要作用
A:____ B:____ C:_____
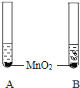
(2)鉴别水和过氧化氢两瓶无色液体,请填写有关内容:
实验步骤 | 实验现象 | 实验结论 |
1.将等体积的两种无色液体分别加入A、B两个试管中。 2.分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象。 | A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是_____; |
(3)探究影响过氧化氢分解速率的因素?(以下实验中使用的溶液都是过氧化氢溶液)
探究实验一:浓度对化学反应速率的影响
实验步骤 | 现 象 |
1、取一支试管加入5g克5%的溶液,然后加入1g二氧化锰。 | 缓慢有少量气泡冒出 |
2、另取一支试管加入___克 15%的溶液,再加入1g二氧化锰。 | 迅速有大量气泡冒出 |
为保证探究结果的准确性,实验步骤2的横线上的数字是____,通过实验发现:当其他条件相同时,过氧化氢的浓度越高,分解的速率_____。
探究实验二:
序 号 | 溶液 浓度 | 溶液质量/g | 温度/℃ | 收集的氧气体积/ml | 反应时间/S |
1 | 30% | 12 | 40 | 125 | 148 |
2 | 30% | 12 | 90 | 125 | 82 |
此实验的目的是探究____ 对过氧化氢分解速率的影响。